Μέρος 1: Γιατί οι φυτικές ορμόνες κυτταροκινίνης έχουν νευροπροστατευτική δράση σε in vitro μοντέλα της νόσου του Πάρκινσον;
Mar 22, 2022
Επαφή:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Pls κάντε κλικ εδώ στο Μέρος 2

Το Cistanche έχει πολύ καλή νευροπροστατευτική δράση
Γκαμπριέλ Γκονζάλες 1,2 , Τζιαρί Γκροζ 1, Κόζιμο Βάλτερ Ντ' Ακούντο 1, Πετρ Κα Ινοβσκ2 και Μίροσλαβ Στρνάντ1,2,*
1. Εργαστήριο Ρυθμιστών Ανάπτυξης, Ινστιτούτο Πειραματικής Βοτανικής της Τσεχικής Ακαδημίας Επιστημών,
και Σχολή Θετικών Επιστημών, Πανεπιστήμιο Palacký, Šlechtitel °u 27, CZ-78371 Όλομουτς, Τσεχική Δημοκρατία·
Gonzalez.gabriel@seznam.cz (Γ.Γ.)· jiri.gruz@upol.cz (J.G.); waldacun@gmail.com (C.W.D.)
2. Τμήμα Νευρολογίας, Πανεπιστημιακό Νοσοκομείο Olomouc και Τμήμα Ιατρικής και Οδοντιατρικής,
Πανεπιστήμιο Palacký Olomouc, CZ-775 20 Όλομουτς, Τσεχική Δημοκρατία; Petr.Kanovsky@fnol.cz
* Αλληλογραφία: miroslav.strnad@upol.cz; Τηλ.: +420-585-634-850
Αφηρημένος:Κυτοκινίνεςείναι φυτοορμόνες με βάση την αδενίνη που ρυθμίζουν βασικές διεργασίες στα φυτά, όπως η κυτταρική διαίρεση και διαφοροποίηση, η ανάπτυξη ριζών και βλαστών, η κορυφαία κυριαρχία, η διακλάδωση και η βλάστηση των σπόρων. Σε προκαταρκτικές μελέτες, έχουν επίσης δείξει προστατευτικές δραστηριότητες κατά των ανθρώπινων νευροεκφυλιστικών ασθενειών. Για να επεκτείνουμε τη γνώση της προστασίας (προστατευτικής δραστηριότητας) που προσφέρουν, διερευνήσαμε δραστηριότητες φυσικώνκυτοκινίνεςκατά της τοξικότητας που προκαλείται από τη σαλολινόλη (SAL) (αΝόσος του Πάρκινσονμοντέλο) και ο θάνατος που προκαλείται από το γλουταμινικό (Glu)νευρώνας-όπως τα ντοπαμινεργικά κύτταρα SH-SY5Y. Διαπιστώσαμε ότι η κινετίνη-3-γλυκοζίτη, η ριβοσίδη της σις-ζεατίνης και η Ν6-ισοπεντενυλο αδενοσίνη ήταν ενεργές στο μοντέλο PD που προκαλείται από το SAL. Επιπλέον, η trans-, cis-ζεατίνη και η κινετίνη μαζί με τον χηλικό παράγοντα σιδήρου δεφεροξαμίνη (DFO) και τον αναστολέα νεκροστατίνης νεκροστατίνης 1 (NEC-1) μείωσαν σημαντικά τα ποσοστά κυτταρικού θανάτου στο μοντέλο που προκαλείται από το Glu. Οι δοκιμασίες γαλακτικής αφυδρογονάσης αποκάλυψαν ότι ηκυτοκινίνεςπαρέχονται χαμηλότερανευροπροστατευτικήδραστηριότητα από το DFO και το NEC-1. Επιπλέον, μείωσαν τις δραστηριότητες της αποπτωτικής κασπάσης-3/7 λιγότερο έντονα από την DFO. Ωστόσο, ηκυτοκινίνεςείχαν πολύ παρόμοιες επιδράσεις με το DFO και το NEC-1 στην παραγωγή ριζών υπεροξειδίου. Συνολικά, έδειξαν προστατευτική δραστηριότητα στο μοντέλο που προκαλείται από το SAL τουπαρκινσονικήΝευρωνικήο κυτταρικός θάνατος και το μοντέλο οξειδωτικής βλάβης που προκαλείται από το Glu κυρίως με τη μείωση του οξειδωτικού στρες.
Λέξεις-κλειδιά: κυτοκινίνη; φυτοορμόνες. νευροπροστασία. κύτταρα SH-SY5Y που μοιάζουν με νευρώνες. κυτταροτοξικότητα. σαλσολινόλη. γλουταμινικό; οξειδωτικό στρες. Νόσος του Πάρκινσον

φυτό cistancheσχετικά με τις επιπτώσεις στιςΝευροπροστασία
1. Εισαγωγή
Νόσος του Πάρκινσον(PD) είναι η δεύτερη πιο κοινή κινητική νευροεκφυλιστική νόσος και ο αριθμός των παγκοσμίως διαγνωσμένων περιπτώσεων αναμένεται να αυξηθεί από 6 εκατομμύρια το 2015 σε περισσότερα από 12 εκατομμύρια έως το 2040 [1]. Χαρακτηρίζεται από κινητικά συμπτώματα που συνδέονται με ειδική εκφύλιση και απώλεια περίπου 30-70% των ντοπαμινεργικών (DA)Νευρώνεςστη μέλαινα ουσία nigra pars compacta και τις προεξοχές τους στο ραβδωτό σώμα [2,3]. Μερικά, από τα πολλά, γνωστά μοριακά χαρακτηριστικά γνωρίσματα της ΝΠ περιλαμβάνουν ενισχυμένο οξειδωτικό και νιτροδωτικό στρες, μιτοχονδριακή δυσλειτουργία [4–7], εκτιτοτοξικότητα [8], δυσλειτουργία ουβικουιτίνης/πρωτεασομικού συστήματος [9] και νευροφλεγμονή [10]. Οι τρέχουσες θεραπείες έχουν διάφορες ανεπιθύμητες παρενέργειες και προσφέρουν μόνο συμπτωματική ανακούφιση [11], επομένως υπάρχουν έντονες προσπάθειες για την ανάπτυξη φαρμάκων με αποτελεσματικές θεραπευτικές επιδράσεις στον εκφυλισμό της DAΝευρώνες. Οι πόροι που μπορεί να βοηθήσουν τέτοιες προσπάθειες περιλαμβάνουν φυσικές ενώσεις που τείνουν να έχουν λιγότερες παρενέργειες. Μεταξύ άλλων, ουσίες από Ginkgo biloba (ginkgetin, ginkgolide, bilobalide), ginseng (ginsenosides) και φλαβονοειδή (baicalein, kaempferol, ρουτίνη και λουτεολίνη) έχουν επιδείξει ευρεία προστατευτική δράση σε διάφορα μοντέλα in vitro (συμπεριλαμβανομένης της κυτταρικής σειράς ανθρώπινου νευροβλαστώματος SH-SY5Y) και in vivo μοντέλα PD που επάγονται από διχλωριούχο 1,1'-διμεθυλο-4,4'-διπυριδινίου (paraquat), 1-μεθυλο-4-φαινυλο-1,2,3,6-τετραϋδροπυριδίνη (MPTP), 1-μεθυλο-4-φαινυλοπυρίδιο (MPP+), και 6-υδροξυδοπαμίνη (6-OHDA) [12].
Η μελέτη που παρουσιάζεται εδώ επικεντρώθηκε στις επιδράσεις μιας κατηγορίας φυσικών φυτοορμόνες που ονομάζονταικυτοκινίνες(CKs), και οι μεταβολίτες τους, οι οποίοι είναι γνωστοί ρυθμιστές της κυτταρικής διαίρεσης, της ανάπτυξης, της διαφοροποίησης και της γήρανσης των φύλλων στα φυτά [13]. Δομικά, τα CK είναι παράγωγα αδενίνης που υποκαθίστανται στη θέση Ν6 είτε με πρένιο (ισοπεντενύλιο) είτε με αρωματικό sidechain. Οι φυσικές μορφές περιλαμβάνουν την 6-(Ε)-4-υδροξυ-3-μεθυλοβουτ-2-ενυλαμινοπουρίνη (trans- ζεατίνη, tZ), το 6-(Z)-ισομερές της (cis-ζεατίνη, cZ), την N6-ισοπεντενυλική αδενίνη (iP), την 6-βενζυλική αμινο-πουρίνη (BAP), την 6-φουρφουρυλαμινοπουρίνη (κινετίνη, Κ), και τα ορθο-, μετα-, και παρα-υδροξυλιωμένα ή μεθοξυλιωμένα παράγωγα της BAP, που ονομάζονται τοπολίνες (oT, mT, pT, MeoT, MemT, MepT). Διάφορα 9-ριβοσίδια, 9-νουκλεοτίδια, καθώς και 7-, 9 και Ο-γλυκοζίτες αυτών των μορφών εμφανίζονται επίσης συχνά, όπως φαίνεται στον Πίνακα 1. Εκτός από τους ιθαγενείς ρόλους τους στα φυτά, τα CKs έχουν δείξει ισχυρή αντιοξειδωτική δράση μυρμηγκιών προς τα αντιδραστικά είδη οξυγόνου (ROS) που παρέχει προστασία σε διάφορα in vitro μοντέλα στρες των διαταραχών που σχετίζονται με τη γήρανση [14].
Πίνακας 1. Δομέςκυτοκινίνεςκαι τους θετικούς παράγοντες ελέγχου.
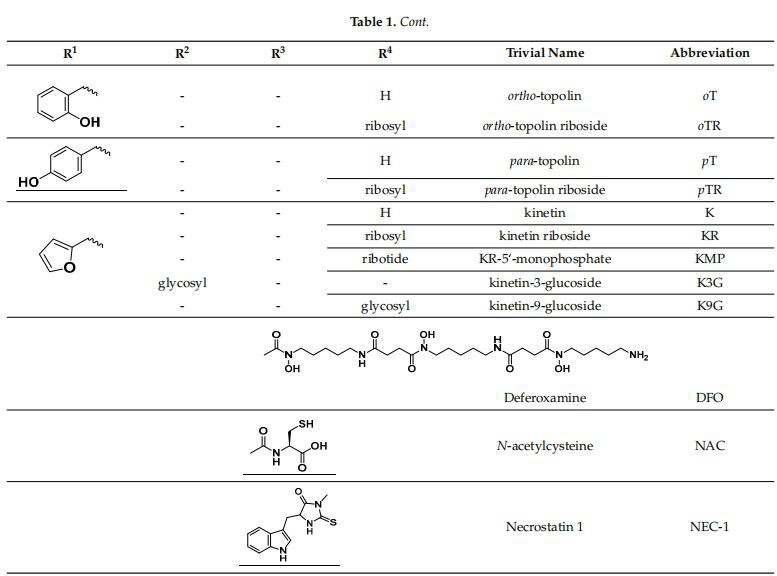
Συγκεκριμένα, οι CKs φέρεται να έχουν κυτταροπροστατευτική δράση σε μοντέλα όπως ο κυτταρικός θάνατος των ανθρώπινων ινοβλαστών που προκαλείται από το H2O2 [15] και το γλυκοξιδικό στρες που προκαλείται από D-γαλακτόζη στα αστροκύτταρα αρουραίων [16]. Το πιο σημαντικό, σε αυτό το πλαίσιο, έχουν δείξεινευροπροστατευτικήεπιδράσεις σε μοντέλα που σχετίζονται με νευροεκφυλιστικές ασθένειες όπως η οικογενής νόσος PD, ο αναστολέας πρωτεασώματος MG 132 ή η τοξικότητα που προκαλείται από H2O2 στα κύτταρα SH-SY5Y [17], η οξειδωτική βλάβη που προκαλείται από το glu του ιππόκαμπου ποντικού HT22Νευρωνικήκύτταρα [18], και το κυτταρικό μοντέλο PC12 της νόσου του Huntington [19]. Άλλες μελέτες δείχνουν ότι οι προστατευτικές δραστηριότητες των CKs περιλαμβάνουν τόσο άμεση [20,21] όσο και έμμεση [15,16,22] διαμόρφωση των κυτταρικών οξειδοαναγωγικών συστημάτων. Εκτός από τις χαρακτηριστικές αντιοξειδωτικές δραστηριότητες των CKs, σύμφωνα με πληροφορίες, έχουν ρυθμιστικές επιδράσεις στα μιτοχόνδρια που ενισχύουνΝευρωνικήβιωσιμότητα [17]. Επιπλέον, το Κ μπορεί να σταθεροποιήσει το δυναμικό της μιτοχονδριακής μεμβράνης και να αυξήσει την παραγωγή ΑΤΡ, μετριάζοντας έτσι τον θάνατο των κυττάρων HT22 που προκαλείται από το Glu [18]. Ωστόσο, παρά τα ευρήματα σχετικά με τις επιπτώσεις τους σε διάφορα μοντέλα, υπάρχει περιορισμένη γνώση της προστατευτικής δραστηριότητας των CKs στην πιο κοινή (σποραδική) μορφή PD.
Για να αντιμετωπίσουμε το κενό γνώσης που περιγράφηκε παραπάνω, αξιολογήσαμε συστηματικά τις επιδράσεις των φυσικών CKs και των μεταβολιτών τους σε δύο in vitro μοντέλα: Ένα μοντέλο PD που προκαλείται από σαλσολινόλη (SAL) και ένα μοντέλο οξειδωτικής βλάβης που προκαλείται από γλουταμινικό (Glu) σενευρώνας-όπως τα κύτταρα SH-SY5Y. Αυτή η γραμμή χρησιμοποιήθηκε λόγω του ντοπαμινεργικού φαινοτύπου της, της ευαισθησίας στις ντοπαμινεργικές τοξίνες όπως το SAL και του βολικού σχηματισμού σχετικά σταθερών πληθυσμών διαφοροποιημένωνΝευρωνικήκύτταρα με μειωμένους ρυθμούς πολλαπλασιασμού μετά από έκθεση 48 ωρών σε 10 uM all-trans ρετινοϊκό οξύ (ATRA) [23–25].
Νευρώνας-ομοειδή κύτταρα εκτέθηκαν στο ενδο/εξωτοξίνη SAL για να μιμηθούν την παθολογία της PD μέσω δυσλειτουργίας του κυτταρικού οξειδοαναγωγικού συστήματος: Εξάντληση της γλουταθειόνης (GSH) και αναστολή τόσο των δραστηριοτήτων του αντι-οξειδωτικού ενζύμου (δισμουτάση υπεροξειδίου Cu/Zn και καταλάσης) όσο και των μιτοχονδριακών συμπλόκων (I και II), που οδήγησαν σε απόπτωση και νέκρωση [26]. Στο άλλο μοντέλο, το Glu προκαλεί δυνητικά θανατηφόρα οξειδωτική βλάβη από διαταραχή του οξειδοαναγωγικού συστήματος. Και τα δύο μοντέλα στην κυτταρική σειρά SH-SY5Y έχουν χρησιμοποιηθεί στο παρελθόν σε μελέτες νευροπροστασίας [26,27].
Οι κυτταροπροστατευτικές και/ή αντιοξειδωτικές δραστηριότητες που σχετίζονται με εκφυλιστικές διαταραχές των K, iP, BAP, iPR, tZR και των ελεύθερων βάσεων τους έχουν δοκιμαστεί και (όπως περιγράφεται παραπάνω) ορισμένα CKs έχουν βρεθεί να έχουν προστατευτικές δραστηριότητες σεΝευρωνικήΚύτταρα. Ωστόσο, καμία προηγουμένως δημοσιευμένη μελέτη δεν έχει εξετάσει τη δομή-νευροπροστατευτικήσχέση δραστηριότητας (SAR) των φυσικών CKs (Πίνακας 1). Ως εκ τούτου, η μελέτη αυτή πραγματοποιήθηκε για να εξεταστείνευροπροστατευτική(αντι-παρκινσονική) δραστηριότητες σχεδόν όλων των γνωστών φυσικών CK στα επιλεγμένα μοντέλα νευροεκφυλισμού που προκαλούνται από SAL και Glu. Πρώτον, αξιολογήσαμε κάθε μία από τις CKs της ικανότητας απορρόφησης ριζών οξυγόνου (ORAC) και (σε δοκιμές ασφαλείας) κυτταροτοξικότητα προς την κατεύθυνσηνευρώνας-όπως τα κύτταρα SH-SY5Y. Στη συνέχεια, αξιολογήσαμε τις νευροπροστατευτικές επιδράσεις των ενώσεων και την επίδραση στα επίπεδα οξειδωτικού στρες μετρώντας την παραγωγή υπεροξειδίου (O2 .) (dihy- droethidium, DHE assay) και τις δραστηριότητες της αποπτωτικής κασπάσης-3,7. Τα αποτελέσματα παρέχουν τις πρώτες αναφερόμενες συστηματικές ενδείξεις των σχέσεων μεταξύ των φυσικών δομών των ΚΚ καινευροπροστατευτικήΔραστηριότητες.

Σιστάντσε χέρμπαέχει ένα πολύ καλόνευροπροστατευτικήεπίδραση
2. Αποτελέσματα και συζήτηση
2.1. Ικανότητα απορρόφησης ριζών οξυγόνου (ORAC) των κυτοκινινών
Καθώς οι νευροεκφυλιστικές ασθένειες σχετίζονται με αυξημένο οξειδωτικό στρες, η αντιοξειδωτική δράση παίζει βασικό ρόλο στην άμυνα τουΝευρωνικήΚύτταρα. Για να εκτιμηθεί το βιολογικό δυναμικό των CKs από αυτή την άποψη, η αντιοξειδωτική ικανότητα προσδιορίστηκε από το ORAC, το οποίο χρησιμοποιείται συνήθως για τον προσδιορισμό της αντιοξειδωτικής ικανότητας των ουσιών [28]. Η αντιοξειδωτική ικανότητα εκφράστηκε ως ισοδύναμα Trolox (TE), τα οποία καθορίζουν την αποτελεσματικότητα (χαμηλότερη έως υψηλότερη) των ενώσεων από το Trolox σε ίση ομομορφική βάση. Τα αποτελέσματα, που παρουσιάζονται στον Πίνακα 1, δείχνουν ότι οι τοπολίνες (oT, mT και pT) και τα ριβοσίδια τους (oTR, mTR, pTR) έχουν υψηλές αντιοξειδωτικές δράσεις, οι οποίες πιθανώς σχετίζονται στενά με το πλούσιο σε ηλεκτρόνια σύστημα του υποκαταστάτη C6-υδροξυβενζυλίου αμινο. Παρά τις υψηλές τιμές ORAC, οι τοπολίνες δεν είχαν υψηλέςνευροπροστατευτικήδραστηριότητα. Ωστόσο, αρκετά ετεροαρωματικά CKs, συμπεριλαμβανομένης της Κ (Ν6-φουρφουρυλαμινοπουρίνης) και της μη αρωματικής cis-ζεατίνης-O-γλυκοζίτη (cZOG), η οποία έχει υποκαταστάτη 4-υδροξυ-3-μεθυλοβουτ-2-εν-1-υλο)αμινο, έδειξαν επίσης υψηλή αντιοξειδωτική ικανότητα (Πίνακας 2). Άλλοι μεταβολίτες της CK—συμπεριλαμβανομένης της κινετίνης-3-γλυκοζίτη (K3G), της ριβοζίδης κινετίνης 5<-monophosphate (kmp),="" kinetin-9-glucoside="" (k9g),="" and="" trans-zeatin=""><- monophosphate="" (tzmp)—had="" moderate="" antioxidant="" activity.="" all="" the="" others="" had="" detectable="" capacity="" except="" bap.="" these="" results="" confirm="" previous="" findings="" that="" ip,="" pt,="" k="" can="" act="" as="" direct="" radical="" scavengers,="" but="" conflict="" with="" the="" previously="" reported="" activity="" of="" bap="" in="" the="" orac="" test="" [20,21].="" to="" conclude,="" these="" compounds="" have="" potential="" in="" the="" treatment="" of="" neurodegenerative="" diseases="" associated="" with="" increased="" oxidative="" stress="">

οφέλη από το στέλεχος cistancheεπίκατά της νόσου του Αλτσχάιμερ
2.2. Διαφοροποίηση των κυττάρων SH-SY5Y
Για να μελετήσετε τα CKs'νευροπροστατευτικήεπιδράσεις, τα κύτταρα νευροβλαστώματος SH-SY5Y (που επιλέχθηκαν για λόγους που έχουν ήδη περιγραφεί [23]) διαφοροποιήθηκαν ανάλογα με την έκθεση σε ATRA 10 uM για 48 ώρες, όπως περιγράφηκε προηγουμένως [23,24]. Στη συνέχεια χρωματίστηκαν χρησιμοποιώντας ένα κιτ χρώσης μεμβράνης για να εξετάσουν τις μορφολογικές διαφορές μεταξύ αδιαφοροποίητων και διαφοροποιημένων κυττάρων. Όπως φαίνεται στο γράφημα 1Α, ηνευρώνας-όπως τα διαφοροποιημένα κύτταρα αναπτύχθηκαν λιγότερο πυκνά, ήταν πιο παρατεταμένα και παρήγαγαν περισσότερους νευρίτες (που υποδεικνύονται από κίτρινα βέλη στο σχήμα) από τα αδιαφοροποίητα κύτταρα. Αυτές οι μορφολογικές αλλαγές που σχετίζονται με τη διαφοροποίηση έχουν παρατηρηθεί προηγουμένως, ακόμη και μετά από μικρότερη έκθεση (24 ώρες) σε ATRA [24,30]. Το πιο σημαντικό, ο αριθμός των νευριτών αυξάνεται δραματικά σε ένα επίπεδο όταν μπορούν να δημιουργήσουν ένα δίκτυο νευριτών. Για το λόγο αυτό, η βιωσιμότητα των κυττάρων μετρήθηκε για να συγκριθεί ο ρυθμός πολλαπλασιασμού των αδιαφοροποίητων και διαφοροποιημένων κυττάρων SH-SY5Y. Η βιωσιμότητα του αδιαφοροποίητου SH-SY5Y ελήφθη ως ο μέγιστος ρυθμός πολλαπλασιασμού. Τα αποτελέσματα που υπάρχουν στο
Το σχήμα 1Β δείχνει ότι το ποσοστό πολλαπλασιασμού (που αξιολογήθηκε από τη δοκιμασία βιωσιμότητας Calcein AM) του SH-SY5Y μειώθηκε κατά 23% μετά από θεραπεία με ATRA 48 ώρες.

Σχήμα 1. (A) Φθορίζουσες μικρογραφίες κυττάρων SH-SY5Y με μεμβράνες χρωματισμένες με τη χρήση κιτ ανάπτυξης Neurite (Invitro-gen™): Έλεγχος, αδιαφοροποίητα κύτταρα (εκτεθειμένα σε διάλυμα εικονικής επεξεργασίας:<0.1% dmso);="" cells="" differentiated="" by="" exposure="" to="" 10="" um="" all-trans="" retinoic="" acid="" (atra)="" for="" 48="" h.="" bars="50" um.="" (b)="" proliferation="" rates="" of="" undifferentiated="" and="" differentiated="" sh-sy5y="" cells:="" numbers="" of="" viable="" cells="" after="" 48="" h="" exposure="" to=""><0.1% dmso="" and="" 10="" um="" atra,="" respectively.="" data="" were="" obtained="" from="" five="" independent="" experiments="" with="" triplicate="" cultures:="" asterisks="" show="" the="" significance="" of="" differences="" in="" numbers="" of="" viable="" cells="" (as="" percentages="" of="" numbers="" of="" undifferentiated="" cells)="" between="" the="" cultures:="" *="" p=""><>
Πίνακας 2. Ικανότητα απορρόφησης ριζών οξυγόνου (ORAC) της δοκιμασμένηςκυτοκινίνες(CK) εκφραζόμενα ως ισοδύναμα Trolox (TE) σε ίση ομομοριακή βάση. Τα ονόματα, οι συντομογραφίες και οι δομές των CK παρουσιάζονται στο Σχήμα 1.

2.3. Κυτταροτοξικότητα των κυτοκινινών έναντι κυττάρων SH-SY5Y που μοιάζουν με νευρώνες
Σε δοκιμές της πιθανής κυτταροτοξικότητας των CKs με τη δοκιμασία βιωσιμότητας Calcein AM [31] οι περισσότεροι έδειξαν χαμηλή τοξικότητα προς τηννευρώνας-όπως τα κύτταρα SH-SY5Y. Η μείωση της βιωσιμότητας κάτω από το 90% θεωρήθηκε ως όριο για νευροτοξική δράση. Οι μόνες δύο εξαιρέσεις ήταν kr (11,9%) και pTR (10,5%), σύμφωνα με προηγούμενα ευρήματα ότι ορισμένεςκυτοκινίνημεταβολίτες, ιδιαίτερα ριβοσίδια, μπορεί να έχουν κυτταροτοξικές επιδράσεις [32]. Άλλα ριβοσίδια, όπως η cZR, η iPR, η oTR, η mTR, δεν προκάλεσαν εμφανή μείωση τηςνευρώνας-όπως η βιωσιμότητα των κυττάρων SH-SY5Y (Πίνακας 3). Το DFO [33,34] και το NEC-1 [35,36] που χρησιμοποιούνται ως θετικοί μάρτυρες στο in vitro μοντέλο μας αποδείχθηκαν επίσης από άλλες μελέτες σε κύτταρα SH-SY5Y ότι είναι μη τοξικά. Συμπερασματικά, κυρίως τα παράγωγα KR και pTR παρουσίασαν χαμηλότερη βιωσιμότητα από το 90% και ως εκ τούτου θεωρήθηκαν λιγότερο ενδιαφέροντα για περαιτέρω αξιολόγηση και στα δύο in vitro μοντέλα νευροεκφυλισμού.
Πίνακας 3. Κυτταρική βιωσιμότητα τουνευρώνας-όπως τα κύτταρα SH-SY5Y μετά από έκθεση σεκυτοκινίνεςγια 24 ώρες. Η βιωσιμότητα εκφράζεται ως ποσοστό του ελέγχου DMSO.

2.4. Ταυτοποίηση των νευροπροστατευτικών κυτοκινινών στο επαγόμενο από SAL μοντέλο PD
Για αυτές τις δοκιμές,ΝευρωνικήΤα κύτταρα SH-SY5Y διαφοροποιήθηκαν για 48 ώρες και στη συνέχεια συν-υποβλήθηκαν σε συν-επεξεργασία με 500 uM SAL και κάθε CK σε τρεις συγκεντρώσεις (0,1, 1, 10 uM). Όπως φαίνεται από τη διακεκομμένη γραμμή στο Σχήμα 2Α, η εφαρμογή του NEUROTOXIN SAL στα 500 uM μείωσε τη βιωσιμότητα των διαφοροποιημένων κυττάρων SH-SY5Y, σύμφωνα με τη δοκιμασία Calcein AM, κατά 30%. Ν-ακετυλοκυστεΐνη (NAC) χρησιμοποιήθηκε ως θετικός μάρτυρας σε αυτές τις δοκιμές λόγω της προηγουμένως αναφερθείσας νευροπροστατευτικής δράσης της στο ίδιο SH-SY5Y κυττάρων με βάση in vitro μοντέλο [37]. Συγκεντρώσεις 10, 100 και 1000 uM NAC χρησιμοποιήθηκαν για να προκαλέσουν μερική ή σχεδόν πλήρη ανάκτηση στο μοντέλο SAL. Nac ήταν σε θέση να αυξήσει τη βιωσιμότητα των κυττάρων σε 100 uM και 1 mM συγκέντρωση, που αντιστοιχεί σε 83.39 ± 1.74% και 89.21 ± 2.89%, αντίστοιχα. Η προστατευτική δραστηριότητα του NAC στα 100 uM (που υποδεικνύεται από τη διακεκομμένη γραμμή στο Σχήμα 2Α) χρησιμοποιήθηκε ως όριο ισχύος για την επιλογή CK για περαιτέρω δοκιμές. Σύμφωνα με αυτή τη ρύθμιση, οι βιολογικά σημαντικές νευροπροστατευτικές δραστηριότητες έχουν παρατηρηθεί με K3G σε 10 uM (81,84 ± 2,36%), cZR σε 0,1 uM (81,14 ± 2,30%) και 1 uM (81,53 ± 2,24%) και iPR σε 1 uM (82,43 ± 2,51%). Έτσι, iPR και cZR ήταν αποτελεσματικά νευροπροστατευτικά σε χαμηλότερες μικρο ή υπο-μικρομοριακές συγκεντρώσεις από το NAC. ΟκυτοκινίνηΟ έλεγχος αποκάλυψε επίσης ότι πολλοί άλλοι μεταβολίτες μπορούν να αυξήσουν μέτρια τη βιωσιμότητα των διαφοροποιημένων κυττάρων SH-SY5Y που εκτίθενται στο SAL. Ωστόσο, ορισμένα δοκιμασμένα CK (συμπεριλαμβανομένων των tZR, tZMP, mT, mTR, pT και pTR) είχαν πολύ μικρή προστατευτική επίδραση.

Εικόνα 2. α)Νευροπροστατευτικήδραστηριότητα τηςκυτοκινίνεςκαι Ν-ακετυλοκυστεΐνη (NAC) σε SAL-επαγόμενο μοντέλο της PD σενευρώνας-όπως τα κύτταρα SH-SY5Y. Η διακεκομμένη γραμμή δείχνει το όριο εφέ NAC στο οποίοκυτοκινίνεςεπελέγησαν για περαιτέρω δοκιμές· στη συνέχεια, η διακεκομμένη γραμμή μετρά τον αριθμό των ζωντανών κυττάρων στη δοκιμασία Calcein AM μετά την επεξεργασία των κυττάρων με 500 uM SAL· υγιή κύτταρα ελέγχου (CTR, DMSO< 0.1%).="" triplicates="" in="" at="" least="" three="" separated="" days.="" (b)="" normalized="" sh-sy5y="" cell="" death="" after="" propidium="" iodide="" staining.="" triplicates="" in="" at="" least="" five="" independent="" days.="" *="" p="" compared="" with="" the="" vehicle="" with="" 500="" um="" sal,="" #="" p="" compared="" with="" the="" vehicle="" without="" 500="" um="">
Για να επιβεβαιωθεί, οι πιο δραστικές φυσικές δραστηριότητες CK κατά του PD, τα συνολικά ποσοστά κυτταρικού θανάτου ποσοτικοποιήθηκαν με χρώση ιωδιούχου προπιδίου (PI), η οποία (σε αντίθεση με τις δοκιμές βιωσιμότητας που βασίζονται στο μεταβολισμό των κυττάρων) επισημαίνει μόνο κύτταρα με μειωμένη ακεραιότητα μεμβράνης, πεθαμένα κύτταρα και ήδη νεκρά κύτταρα [38]. Τα αποτελέσματα ομαλοποιήθηκαν σε σχέση με το ποσοστό κυτταρικού θανάτου μετά από θεραπεία μόνο με SAL (που ορίστηκε ως 100%). Όπως φαίνεται στο Σχήμα 2Β, η ουσία θετικού μάρτυρα NAC μείωσε σημαντικά τα ποσοστά κυτταρικού θανάτου τόσο στα 100 όσο και στα 1000 uM (σε 77,3 ± 2,21% και 77,5 ± 4,44%, αντίστοιχα). Συνολικά, το NAC αποδείχθηκε ότι ήταν ένανευροπροστατευτικήμε συγκρίσιμες δραστηριότητες με εκείνες που καταγράφηκαν σε άλλες μελέτες με δοσοεξαρτώμενο τρόπο (στην περιοχή των 50–500 uM) για τα κύτταρα SH-SY5Y [37]. Η δοκιμασία PI έδειξε επίσης ότι τα CKs cZR, K3G και iPR έχουν προστατευτικές δραστηριότητες, ειδικά cZR, γεγονός που μείωσε το ποσοστό κυτταρικού θανάτου σε 71,6 ± 5,08% στα 0,1 uM. Σε αντίθεση με τη cZR, το K3G είχε αντιστρέψει τις δοσοεξαρτώμενες επιδράσεις, με μέγιστη ραδιενέργεια στα 10 uM (μείωση του ποσοστού κυτταρικού θανάτου σε 75,0 ± 3,69%) και η δραστικότητα του NPR κορυφώθηκε στο 1 uM (μειώνοντας το ποσοστό σε 73,9 ± 4,99%). Συνολικά, όπως φαίνεται στο γράφημα 2, τα ΚΚ παρείχαν συγκρίσιμηνευροπροστατευτικήσε 100 uM NAC σύμφωνα με τις δοκιμασίες βιωσιμότητας και κυτταροτοξικότητας. Επιπλέον, οι αποτελεσματικές συγκεντρώσεις CK όπως το cZR και το iPR ήταν πολύ χαμηλότερες από εκείνες του NAC, στις υπο-μικρομοριακές και μικρομοριακές περιοχές. Προηγούμενες παρατηρήσεις που ελήφθησαν μετά από διπλή χρώση με PI και annexin V/PI δείχνουν ότι το K μπορεί να μειώσει την απόπτωση [39], έτσι διερευνήσαμε επίσης τις επιδράσεις των CKs και του NAC στο οξειδωτικό στρες και την ενεργοποίηση της κασπάσης-3,7 (ένας γνωστός δείκτης απόπτωσης).
2.5. Οι κυτοκινίνες μειώνουν τον σχηματισμό ριζών υπεροξειδίου που προκαλείται από το SAL
Το οξειδωτικό στρες (OS) είναι ένας βασικός παθολογικός παράγοντας που συμβάλλει σε αρκετές νευροεκφυλιστικές ασθένειες και τόσο το SAL (σε > 100 uM) όσο και οι τετραϋδροϊσοκινολίνες είναι ισχυροί επαγωγείς os [26,40]. Έτσι, μετρήσαμε επίσης το σχηματισμό υπεροξειδίου (ένα ROS και σημαντικό δείκτη OS) παρουσία SAL με και χωρίς επιλεγμένα CKs ή NAC. Για να διασφαλιστεί ότι το SAL προκάλεσε επαρκή βλάβη του λειτουργικού συστήματος στα κύτταρα SH-SY5Y για την ανίχνευση αποκρίσεων, τα κύτταρα εκτέθηκαν σε 500 uM SAL για 24 ώρες, όπως σε προηγούμενες εργασίες [37] και σύμφωνα με τα ευρήματα που παρουσιάστηκαν παραπάνω. Στη συνέχεια, τα κύτταρα χρωματίστηκαν από διυδροηθίδιο (DHE) για να ανιχνεύσουν το σχηματισμό ριζών υπεροξειδίου [41,42]. Όπως μπορεί να φανεί στο Σχήμα 3Α, τα κύτταρα παρατηρήθηκαν οπτικά μετά την επισήμανση με DHE (η οποία παρέχει κόκκινα σήματα φθορισμού μετά από αντίδραση με υπεροξείδιο). SAL προκάλεσε μια σαφή αύξηση του φθορισμού DHE, σε σχέση με τα επίπεδα στον έλεγχο και NAC-επεξεργασμένα κύτταρα. Επιπλέον, τρία CK (cZR, K3G και iPR) είχαν παρόμοια οπτικά εφέ με το NAC (100 uM) στον φθορισμό DHE. Επιπλέον, ο φασματοφωτομετρικός ποσοτικός προσδιορισμός σε σχέση με τα επίπεδα που ανιχνεύθηκαν σε κύτταρα που υποβλήθηκαν σε θεραπεία μόνο με SAL (που ορίστηκε ως 100%), ήταν σύμφωνη με την παρατήρηση μικροσκοπίας. Όπως φαίνεται στο Σχήμα 3Β, το κανονικοποιημένο επίπεδο υπεροξειδίου σε υγιή κύτταρα ελέγχου (CTR) ήταν μικρότερο από 39% και η θετική ουσία μάρτυρας NAC παρείχε μέτρια έως πλήρη μείωση της παραγωγής ROS που προκαλείται από SAL στα 100 και 1000 uM (σε 76,3 ± 4,33 και 44,3 ± 5,12%), υποδηλώνοντας ότι η εξάντληση της γλουταθειόνης (GSH) παίζει βασικό ρόλο στο μοντέλο [26]. Είναι ενδιαφέρον ότι το SAL προκάλεσε δραματικές μειώσεις στις περιεκτικότητες GSH των κυττάρων SH-SY5Y συνοδευόμενες από αύξηση του OS, σε επίπεδα παρόμοια με αυτά που παρατηρήθηκαν προηγουμένως σε μια μελέτη που κατέγραψε επίσης επιδράσεις με τη μεσολάβηση του NAC στη βιωσιμότητα των κυττάρων, τον κυτταρικό θάνατο και την περιεκτικότητα σε γλουταθειόνη [43]. Τα αποτελέσματα που παρουσιάζονται εδώ δείχνουν ότι το NAC μείωσε επίσης το σχηματισμό ριζών υπεροξειδίου σε βασικά επίπεδα (δηλαδή, επίπεδα σε μάρτυρες που έχουν υποστεί επεξεργασία με DMSO). Τα ριβοσίδια CK ελέγχθηκαν σε ενεργές συγκεντρώσεις (0,1–1 uM) μαζί με K3G και μείωσαν σημαντικά την περιεκτικότητα των κυττάρων σε ριζικές ρίζες υπεροξειδίου στα ακόλουθα επίπεδα (σε σχέση με εκείνα των κυττάρων που έλαβαν μόνο SAL): cZR 80,34 ± 5,99% στα 0,1 uM. Το K3G 77,1 ± 4,89% στα 10 uM. iPR 79.2 ± 5.91% σε 1 uM, συγκρίσιμη με τις επιδράσεις των 100 uM NAC. Συλλογικά, οι ορθογώνιες επιδείξεις δείχνουν έντονα ότι η ισχυρή δραστηριότητα κατά του λειτουργικού συστήματος παίζει βασικό ρόλο στις προστατευτικές επιδράσεις του NAC και των CK στο μοντέλο PD που προκαλείται από το SAL. Μια συσχέτιση μεταξύ της βελτίωσης του OS και της νευροπροστασίας έχει επίσης παρατηρηθεί από άλλους συγγραφείς [29], και αρκετές μελέτες έχουν διαπιστώσει ότι το K και το BAP μπορούν να βελτιώσουν άμεσα τις δραστηριότητες του OS [44] μέσω του σχηματισμού συμπλόκων με ιόντα Cu2+, με αποτέλεσμα τη δραστηριότητα που μοιάζει με δισμουτάση υπεροξειδίου [45,46]. Ωστόσο, τα CK έχουν επίσης περιγραφεί ως έμμεσα αντιοξειδωτικά με επιδράσεις που μεσολαβούνται από την επαγωγή του πυρηνικού παράγοντα ερυθροειδούς 2 που σχετίζεται με τον παράγοντα 2 (NRF2) της οδού αντιοξειδωτικής απόκρισης (iPR) [22] ή τη μερική αποκατάσταση των δραστηριοτήτων υπεροξειδάσης της γλουταθειόνης και του SOD (K) [16]. Επιπλέον, ο Κ φέρεται να έχεινευροπροστατευτικήδραστηριότητες κατά του τραυματισμού της OS που προκαλείται από το H2O2 σε κύτταρα SH-SY5Y [17]. Και οι δύο τύποι αναφερόμενης αντι-ROS δραστικότητας των CKs θα μπορούσαν ενδεχομένως να εξηγήσουν τις επιδράσεις των cZR, K3G και iPR στη μείωση των ριζών υπεροξειδίου στο μοντέλο PD κυττάρων SH-SY5Y που προκαλείται από SAL [47–50].

Εικόνα 3. (Α) Μικροφωτογραφίες που δείχνουν το οξειδωτικό στρες που προκαλείται από το SAL και τις δραστηριότητες μείωσης του οξειδωτικού στρεςκυτοκινίνεςσε ανθρώπινες διαφοροποιημένεςνευρώνας-όπως τα κύτταρα SH-SY5Y που απεικονίζονται με μικροσκοπία φθορισμού μετά από επισήμανση διυδροαιθιδίου (DHE). Ράβδοι = 50 ουμ. Οι εικόνες δείχνουν κύτταρα που έχουν υποβληθεί σε θεραπεία με διάλυμα DMSO (μάρτυρες), 500 uM σαλσολινόλης (SAL) μόνο και συνδυασμούς 500 uM SAL και 1000 uM NAC (+NAC), 0,1 uM cZR (+cZR). 10 uM K3G (+K3G), 1uM iPR (+iPR) για 24 ώρες πριν από τη χρώση με DHE. Β) σχηματισμός ριζών υπεροξειδίου που προκαλείται από το SAL καικυτοκινίνηή Ν-ακετυλοκυστεΐνη (NAC) προστατευτική δραστηριότητα. Το γράφημα δείχνει την ποσοτικοποίηση των χρωματισμένων κυττάρων DHE χρησιμοποιώντας τον αναγνώστη μικροπλάκας Infinite M200 Pro (Tecan, Αυστρία). Τριπλασιάζεται σε τουλάχιστον πέντε ανεξάρτητες ημέρες. * P σε σύγκριση με το όχημα με 500 uM SAL, # P σε σύγκριση με το όχημα χωρίς 500 uM SAL.

