Ανακούφιση των συμπτωμάτων σε ασθενείς που υποβάλλονται σε μακροχρόνια αιμοκάθαρση: Εστίαση στον κνησμό που σχετίζεται με τη χρόνια νεφρική νόσο
May 31, 2023
Αφηρημένη
Από την ανακάλυψη της θεραπείας υποκατάστασης νεφρού, οι αυξήσεις στο προσδόκιμο ζωής για ασθενείς με νεφρική νόσο τελικού σταδίου έχουν περιοριστεί. Ωστόσο, οι ασθενείς έχουν γίνει ολοένα και πιο έντονοι ότι, αν και η θνησιμότητα και το προσδόκιμο ζωής έχουν σημασία για αυτούς, η ποιότητα της ζωής τους, και ιδιαίτερα η ανακούφιση των συμπτωμάτων που σχετίζονται με τη θεραπεία τους, είναι σε πολλές περιπτώσεις πιο σημαντική. Η πλειονότητα των συμπτωμάτων και των ανεπιθύμητων ενεργειών που σχετίζονται με την αιμοκάθαρση δεν έχουν επί του παρόντος εγκεκριμένες θεραπείες σε αυτόν τον πληθυσμό ασθενών, με τις λίγες διαθέσιμες θεραπείες που χρησιμοποιούνται εκτός ετικέτας, συχνά χωρίς αποδεδειγμένη αποτελεσματικότητα, αλλά εξακολουθούν να προσθέτουν περαιτέρω δυσμενείς επιπτώσεις στην τρέχουσα επιβάρυνση των συμπτωμάτων του ασθενούς . Αυτό το άρθρο θα επεξηγήσει πώς η κατανόηση της παθοφυσιολογίας ενός μεμονωμένου, ιδιαίτερα επιβαρυντικού συμπτώματος της αιμοκάθαρσης (χρόνιος κνησμός που σχετίζεται με την νεφρική νόσο) οδήγησε στον σχεδιασμό, την ανάπτυξη και την έγκριση από τους κανονισμούς μιας θεραπείας για αυτό το σύμπτωμα. Η οδός που περιγράφεται εδώ μπορεί να εφαρμοστεί και σε άλλα συμπτώματα που σχετίζονται με την αιμοκάθαρση, πράγμα που σημαίνει ότι αν δεν μπορούμε να προσθέσουμε χρόνια στη ζωή των ασθενών, μπορούμε τουλάχιστον να προσθέσουμε ζωή στα υπόλοιπα χρόνια τους.
Λέξεις-κλειδιά
κνησμός που σχετίζεται με χρόνια νεφρική νόσο, αιμοκάθαρση, difelikefalin, ποιότητα ζωής, ανακούφιση από τα συμπτώματα.

Κάντε κλικ εδώ για να λάβετετα οφέλη του Cistanche
Εισαγωγή
Αυτό το άρθρο θα απεικονίσει τον σχεδιασμό, την ανάπτυξη και την ρυθμιστική έγκριση μιας θεραπείας για ένα μεμονωμένο, ιδιαίτερα επιβαρυντικό σύμπτωμα της αιμοκάθαρσης [χρόνιος κνησμός που σχετίζεται με την νεφρική νόσο (CKD-aP)]. Αυτό επιτεύχθηκε μέσω της αναγνώρισης της σημασίας της διαχείρισης των συμπτωμάτων CKD-aP στους ασθενείς και της κατανόησης της υποκείμενης παθοφυσιολογίας του συμπτώματος. Αυτό επέτρεψε την ανάπτυξη μιας θεραπείας για τη στόχευση της CKDaP, χρησιμοποιώντας κλινικές δοκιμές ειδικά σχεδιασμένες για τη μέτρηση του αντίκτυπου και της βελτίωσης της CKD-aP. Τα αποτελέσματα που αναφέρθηκαν από τον ασθενή (PROs) χρησιμοποιήθηκαν σε όλες τις δοκιμές, επιτρέποντας στους ρυθμιστές να εκτιμήσουν την αξία αυτής της θεραπείας σε αυτόν τον πληθυσμό ασθενών και, ως εκ τούτου, οδήγησαν σε ρυθμιστική έγκριση - ένα βασικό σημείο στην οδό για την πρόσβαση των ασθενών (Εικ. 1) [1] .
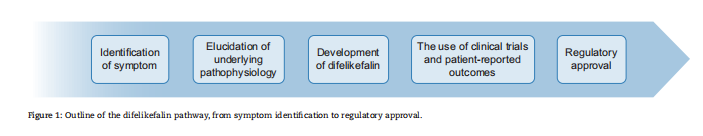
Η επιβάρυνση των συμπτωμάτων και η σημασία της για τους ασθενείς
Σε σύγκριση με τον γενικό πληθυσμό, η ποιότητα ζωής που σχετίζεται με τη σωματική υγεία (QoL) σε ασθενείς με ΧΝΝ [2] και σε άτομα με ΧΝΝ που υποβάλλονται σε θεραπεία υποκατάστασης νεφρού [3] είναι σημαντικά μειωμένη. Επιπλέον, η επιβάρυνση των συμπτωμάτων είναι υψηλή [4, 5], με έως και τους μισούς ασθενείς να αναφέρουν τουλάχιστον ένα σύμπτωμα ως σοβαρό ή συντριπτικό [6]. Η αυξανόμενη αναγνώριση της ανάγκης ανακούφισης των συμπτωμάτων σε ασθενείς που υποβάλλονται σε αιμοκάθαρση προσφέρει μια ευκαιρία να αντιμετωπιστεί αυτό με έναν επιστημονικά ισχυρό τρόπο.
Αυτή η έλλειψη ενσωμάτωσης των προτεραιοτήτων των ασθενών στα σχέδια θεραπείας είχε ως αποτέλεσμα την ανάπτυξη της πρωτοβουλίας Standardized Outcomes in Nephrology (SONG) [7], στην οποία τα αποτελέσματα της αιμοκάθαρσης ευθυγραμμίστηκαν με τις ανάγκες όλων των ενδιαφερομένων (συμπεριλαμβανομένων ασθενών, φροντιστών, κλινικών γιατρών, ερευνητών, και φορείς χάραξης πολιτικής), με τα SONG-HD [8] και SONG-PD [9] να επικεντρώνονται ειδικά στα βασικά αποτελέσματα που σχετίζονται με τους ενδιαφερόμενους φορείς της αιμοκάθαρσης (HD) και της περιτοναϊκής κάθαρσης (PD), αντίστοιχα. Τα συμπτώματα που αναγνωρίζονται από το SONG-HD ως σημαντικά περιλαμβάνουν κόπωση (βασικό αποτέλεσμα), κατάθλιψη, πόνο, άγχος, κράμπες, κνησμό, ναυτία, σύνδρομο ανήσυχων ποδιών, αναιμία, σεξουαλική λειτουργία και διαταραχές ύπνου. η έλλειψη απόλαυσης του φαγητού, η κινητικότητα, ο χρόνος χωρίς αιμοκάθαρση ή η ικανότητα εργασίας ή ταξιδιού· καθώς και μειωμένη γνωστική λειτουργία, τον αντίκτυπο στην οικογένεια/φίλους, τη νοσηλεία και το αίσθημα ξεπλύματος μετά τη διάγνωση. Άλλες πρωτοβουλίες, όπως η Kidney Health Initiative [10], μια συνεργασία δημόσιου-ιδιωτικού τομέα μεταξύ της Αμερικανικής Εταιρείας Νεφρολογίας και της Υπηρεσίας Τροφίμων και Φαρμάκων των ΗΠΑ, έχουν επίσης επιδιώξει να αναπτύξουν ένα εννοιολογικό πλαίσιο για τους PRO που βασίζονται στα συμπτώματα, συμβάλλοντας στην ανάπτυξη των PRO και των ηλεκτρονικών PRO (ePROs) για την ειδική αξιολόγηση των σωματικών συμπτωμάτων που σχετίζονται με τη θεραπεία HD [11].
Ωστόσο, τα περισσότερα συμπτώματα και ανεπιθύμητες ενέργειες που σχετίζονται με την αιμοκάθαρση δεν έχουν επί του παρόντος εγκεκριμένες θεραπείες σε αυτόν τον πληθυσμό ασθενών, με αποτέλεσμα μια ξεκάθαρη ανικανοποίητη ανάγκη (Πίνακας 1). Η ποιότητα ζωής που σχετίζεται με την υγεία σε ηλικιωμένους ή πιο αδύναμους ασθενείς έχει μάλιστα αναφερθεί ότι είναι παρόμοια σε ασθενείς που επιλέγουν να μην εισέλθουν στην οδό αιμοκάθαρσης, λόγω της σημαντικής επιβάρυνσης των συμπτωμάτων που σχετίζονται με την αιμοκάθαρση [12]. Η σαφής εξαίρεση στην ανεκπλήρωτη ανάγκη για θεραπείες για τις ανεπιθύμητες ενέργειες και τα συμπτώματα της αιμοκάθαρσης είναι η ΧΝΝ-αΡ (και η σχετική επίπτωση στη διαταραχή του ύπνου), για την οποία έχει εγκριθεί πρόσφατα μια ειδική θεραπεία [13].


Επισκόπηση της CKD-aP (επιδημιολογία, αιτιολογία, ανικανοποίητη ανάγκη θεραπείας)
Η CKD-aP είναι μια επικρατούσα και οδυνηρή κατάσταση για ασθενείς με νεφρική ανεπάρκεια που υποβάλλονται σε αιμοκάθαρση [14]. Πρόσφατα δεδομένα από τη διεθνή παρατήρηση Αποτελέσματα Αιμοκάθαρσης και Πρότυπα Πράξης Μελέτη (DOPPS) (φάσες 4–6, 2009–18) διαπίστωσαν ότι το 67 τοις εκατό των ασθενών με HD που ερωτήθηκαν ανέφεραν ότι ενοχλούνταν από κνησμό, με το 37 τοις εκατό να αναφέρει μέτρια έως ακραία συμπτώματα. 15].
Ο κνησμός ως σύμπτωμα της HD έχει μια μοναδική υποκείμενη αιτιολογία σε σύγκριση με τον κνησμό στο γενικό πληθυσμό, πράγμα που σημαίνει ότι οι κοινές παρεμβάσεις για τον κνησμό, όπως οι ενυδατικές κρέμες και τα τοπικά κορτικοστεροειδή [16], είναι συχνά αναποτελεσματικές σε ασθενείς με νεφρική ανεπάρκεια [17].
Η CKD-aP μπορεί να μειώσει σημαντικά την ποιότητα ζωής των ασθενών που υποβάλλονται σε HD και μπορεί να αναστείλει την ικανότητά τους να εργαστούν ή να διατηρήσουν μια ενεργή κοινωνική ζωή [14, 17]. Επίσης, σχετίζεται με χειρότερα κλινικά αποτελέσματα, συμπεριλαμβανομένου αυξημένου κινδύνου λοιμώξεων και υψηλότερου ποσοστού νοσηλειών και θνησιμότητας [15]. Ωστόσο, παρά αυτές τις αρνητικές πτυχές, η CKD-aP παραμένει υπο-αναγνωρισμένη από τους γιατρούς [17].
Η CKD-aP συχνά συνυπάρχει με άλλα σωματικά και ψυχο-συναισθηματικά συμπτώματα που παρουσιάζουν ασθενείς με HD, συμπεριλαμβανομένης της κακής ποιότητας ύπνου, της κατάθλιψης, της κόπωσης και του πόνου [17-19], τα οποία μαζί αντιπροσωπεύουν μια σημαντική ομάδα συμπτωμάτων που αντιμετωπίζεται ανεπαρκώς στην κλινική πρακτική [20].

Συμπληρώματα Cistanche και χάπια Cistanche
Παθοφυσιολογία της CKD-ap-Ο κεντρικός ρόλος της οδού των οπιοειδών
Η κατανόηση της παθοφυσιολογίας της CKD-aP ήταν το ουσιαστικό πρώτο βήμα πριν αναπτυχθούν θεραπείες. Αν και η παθοφυσιολογία δεν είναι ακόμη πλήρως κατανοητή, ένας συνδυασμός αρκετών μηχανισμών φαίνεται να συμβάλλει στην εμφάνισή της (Εικ. 2). Αυτές περιλαμβάνουν τη συσσώρευση ουραιμικών τοξινών στο δέρμα και την ενεργοποίηση της μη ισταμινεργικής οδού κνησμού [21], ως αποτέλεσμα περιφερικής νευροπάθειας, δυσρύθμισης του ανοσοποιητικού συστήματος και/ή ανισορροπίας οπιοειδών, με επακόλουθη μικροφλεγμονή και ξηρότητα [22-24].

Η αποσαφήνιση καθενός από αυτούς τους μηχανισμούς έχει παράσχει μια πιθανή οδό θεραπείας για την ανακούφιση της CKD-aP. Ωστόσο, για πολλά χρόνια, οι θεραπείες με επαρκή αποτελεσματικότητα παρέμειναν άπιαστες. Για παράδειγμα, η συσσώρευση και η εναπόθεση τοξινών πιστεύεται τώρα ότι προκαλούν CKD-aP μόνο σε ένα υποσύνολο ασθενών, επειδή η αύξηση της αποτελεσματικότητας της αιμοκάθαρσης (με αποτέλεσμα τη μείωση του Kt/V) και η μείωση του ασβεστίου, της παραθυρεοειδούς ορμόνης ή του φωσφόρου του ορού ανακουφίζουν τον κνησμό μόνο σε μικρό ποσοστό ασθενών [23].
Η περιφερική νευροπάθεια έχει αποδειχθεί ότι προκαλεί κνησμό όταν οι άρρωστοι νευρώνες ενεργοποιούνται ανεξάρτητα παρουσία κνησμογόνων, με την περιφερική νευροπάθεια να είναι ιδιαίτερα διαδεδομένη σε ασθενείς που υποβάλλονται σε αιμοκάθαρση [23]. Ωστόσο, μεγάλης κλίμακας κλινικές δοκιμές θεραπειών που μειώνουν τον πόνο που σχετίζεται με την περιφερική νευροπάθεια δεν έχουν ακόμη δείξει σαφή αποτελεσματικότητα στη ΧΝΝ-aP, και παρόλο που έχουν δείξει κάποια αποτελεσματικότητα σε δοκιμές μικρής κλίμακας [25], μπορεί επίσης να σχετίζονται με νευρολογικές δυσμενείς επιπτώσεις [26].
Η απορρύθμιση του ανοσοποιητικού συστήματος παραμένει ένας πιθανός ρυθμιστής της CKD-aP, καθώς έχουν αναφερθεί αυξημένα επίπεδα ηωσινόφιλων, ιστιοκυττάρων, ισταμίνης και τρυπτάσης. Ωστόσο, τα αντιισταμινικά έχουν περιορισμένη αποτελεσματικότητα κατά του κνησμού [23]. Αναγνωρίζεται ότι η φλεγμονή παίζει βασικό ρόλο στην ευαισθητοποίηση των μικρών νευρικών ινών στο δέρμα που μεταφέρουν την αίσθηση κνησμού στον εγκέφαλο, προκαλώντας το δυσάρεστο σύμπτωμα του κνησμού. Επιπλέον, υψηλά επίπεδα δεικτών συστηματικής φλεγμονής παρατηρούνται σε ασθενείς με ΧΝΝ-α , συμπεριλαμβανομένων των υψηλών επιπέδων Τ κυττάρων και λευκών αιμοσφαιρίων, C-αντιδρώσας πρωτεΐνης, ιντερλευκινών-6 και -2 και φερριτίνης, παράλληλα με χαμηλά επίπεδα λευκωματίνης [27].
Ο ρόλος των υποδοχέων οπιοειδών στην Παθογένεση του κνησμού
Η ανισορροπία στο ενδογενές σύστημα οπιοειδών, που χαρακτηρίζεται από υπερέκφραση σηματοδότησης των υποδοχέων mu-opioid (MOR) και μείωση της σηματοδότησης του υποδοχέα κάπα-οπιοειδών (KOR), έχει εμπλακεί στην παθογένεση του κνησμού στο CKD-aP [28]. Επιπλέον, έχει παρατηρηθεί ανισορροπία έκφρασης MOR και KOR στο δέρμα ασθενών με CKD-aP σε σύγκριση με αυτούς που δεν έχουν κνησμό [29]. Πολλά φάρμακα που δρουν στο MOR και/ή στο KOR έχουν αξιολογηθεί για τη θεραπεία της ΧΝΝ-αΡ, όπως η ναλτρεξόνη, η λοραταδίνη και η ναλβουφίνη. Ωστόσο, σε κλινικές δοκιμές, αυτές έχουν κυρίως αναφέρει περιορισμένη αποτελεσματικότητα [30-34]. Υπάρχουν μερικές ελπιδοφόρες μελέτες με τον μερικό αγωνιστή MOR και αγωνιστή KOR, την υδροχλωρική ναλφουραφίνη, οι οποίες σε υψηλότερες δόσεις κατέδειξαν σημαντικές μειώσεις στην ένταση του κνησμού, όπως μετρήθηκε μέσω της κλίμακας Worst Itch Numeric Rating Scale (WINRS) [34] και της οπτικής αναλογικής κλίμακας [33] . Η ναλφουραφίνη είναι επί του παρόντος εγκεκριμένη για τη θεραπεία της ΧΝΝ-aP στην Ιαπωνία και τη Νότια Κορέα.

Cistanche tubulosa
Η ανάπτυξη του difelikefalin
Το Difelikefalin είναι ένας εκλεκτικός, περιφερικά περιορισμένος αγωνιστής KOR που εγκρίθηκε πρόσφατα στις ΗΠΑ και την Ευρώπη για τη θεραπεία του μέτριου έως σοβαρού κνησμού σε ασθενείς που υποβάλλονται σε HD [13, 35]. Το Difelikefalin αναπτύχθηκε ως ανάλογο ενός ενδογενούς οπιοειδούς πεπτιδίου, της Dynorphin A, το οποίο είναι γνωστό ότι είναι νευροδιαμορφωτής του κνησμού [36]. Παρόμοια με τη Dynorphin A και άλλους αγωνιστές KOR, η difelikefalin πιστεύεται ότι ανακουφίζει τον κνησμό ενεργοποιώντας τα KOR σε περιφερειακούς αισθητήριους νευρώνες και κύτταρα του ανοσοποιητικού [36, 37]. Για να περιοριστεί η πιθανότητα ψυχομιμητικών και δυσφορικών επιδράσεων που παρατηρήθηκαν με ορισμένους άλλους αγωνιστές KOR, επιλέχθηκε η χημική δομή της difelikefalin για να διασφαλιστεί ότι δεν ήταν υπόστρωμα για μεταφορείς πρόσληψης φαρμάκων και ότι δεν θα μεταβολιζόταν σημαντικά. Ο χρόνος ημιζωής της difelikefalin είναι 23–31 ώρες σε ασθενείς που υποβάλλονται σε HD. Οι συγκεντρώσεις της difelikefalin στο πλάσμα μειώθηκαν κατά 70% -80% μετά από HD, με difelikefalin μη ανιχνεύσιμη στο πλάσμα μετά από δύο κύκλους αιμοκάθαρσης [38].
Η αξιολόγηση της ΧΝΝ-αΡ
Οι νεφρολόγοι είναι εξοικειωμένοι με τις μετρήσεις πολλαπλών μεταβλητών που παρακολουθούνται με την πάροδο του χρόνου, ώστε να μπορούν να ποσοτικοποιήσουν με ακρίβεια την εξέλιξη της νόσου. Για παράδειγμα, έχουμε μετρήσεις νεφρικής βλάβης μέσω της αναλογίας λευκωματίνης ούρων προς κρεατινίνη ούρων και μέτρηση νεφρικής ανεπάρκειας μέσω μέτρησης του εκτιμώμενου ρυθμού σπειραματικής διήθησης και μαζί χρησιμοποιούνται για τη σταδιοποίηση της νεφρικής νόσου. Ένα τέτοιο σύστημα σταδιοποίησης επιτρέπει την κατάλληλη χρήση διαγνωστικών διαδικασιών και τη θέσπιση θεραπειών και παρέχει πρόγνωση για τη μελλοντική εξέλιξη της νεφρικής νόσου και των καρδιαγγειακών συμβαμάτων σε τέτοιους ασθενείς. Αντίθετα, τα συμπτώματα δεν έχουν υποβληθεί σε αυτόν τον έλεγχο.
Επειδή δεν υπάρχει εξέταση για μια αλυσίδα συμπτωμάτων, όπως η κρεατινίνη ορού ή μια εξέταση ούρων, είναι απαραίτητο ένα εργαλείο για την παρακολούθηση του συμπτώματος με την πάροδο του χρόνου. Η κλινική επίδραση της ΧΝΝ-αΡ μπορεί να ποσοτικοποιηθεί σε δύο τομείς, τη σοβαρότητα του συμπτώματος και την επίδραση του συμπτώματος στην ευημερία του ασθενούς. Η αξιολόγηση των συμπτωμάτων σε ένα διδιάστατο πλαίσιο - σοβαρότητα και αντίκτυπος - προσφέρεται για την εξέταση της ανταπόκρισης στη θεραπεία. Αν και πολλοί PRO προσπάθησαν να μετρήσουν τη σοβαρότητα της CKD-aP, λίγοι έχουν δοκιμαστεί αυστηρά και η χρήση ενός τέτοιου εργαλείου ήταν ο πρωταρχικός μηχανισμός για την έγκριση των ρυθμιστικών αρχών.
Για τους ασθενείς που έχουν διαγνωστεί με CKD-aP, η αξιολόγηση της σοβαρότητας του κνησμού θα πρέπει επομένως να περιλαμβάνει αξιολόγηση τόσο του επιπέδου της έντασης του κνησμού όσο και της επίδρασης του κνησμού στην ποιότητα ζωής του ασθενούς (Εικ. 3).

Ποσοτικοποίηση της έντασης του κνησμού και της επίδρασης του κνησμού στην ποιότητα ζωής του ασθενούς
Πολλές επικυρωμένες μονοδιάστατες και πολυδιάστατες κλίμακες PRO είναι διαθέσιμες για την αξιολόγηση της έντασης του κνησμού και της ποιότητας ζωής που σχετίζεται με τον κνησμό σε ασθενείς με ΧΝΝ-αΡ [39].
Για παράδειγμα, το ερωτηματολόγιο The Self-Assessed Disease Severity (SADS) είναι επικυρωμένο για την αξιολόγηση του αντίκτυπου της σοβαρότητας της φαγούρας [40, 41]. Αυτό είναι ένα απλό και κατάλληλο εργαλείο που δίνει τη δυνατότητα στους ασθενείς να αυτοαξιολογήσουν γρήγορα την ομοιότητα τριών περιγραφών με συμπτώματα που βιώνουν οι ασθενείς. Έτσι, το ερωτηματολόγιο SADS επιτρέπει στους ασθενείς να ταξινομηθούν σε έναν από τους τρεις «τύπους» ασθενών (Α, Β ή Γ), ανάλογα με την παρουσία γρατσουνιών στο δέρμα, την επίδραση του κνησμού στον ύπνο και την παρουσία διέγερση/λύπη λόγω κνησμού, που κυμαίνεται από τον τύπο Α (ήπιος) έως τον τύπο Γ (σοβαρή). Αν και αυτό το εργαλείο δεν έχει χρησιμοποιηθεί στις κλινικές μελέτες του difelikefalin μέχρι σήμερα, η χρήση του προτείνεται στον αλγόριθμο θεραπείας. σε κλινικές δοκιμές, μπορούμε να επιτύχουμε σχετικά υψηλά ποσοστά ολοκλήρωσης για πιο σύνθετα, πολλαπλών ερωτήσεων εργαλεία QoL, τα οποία μπορεί επίσης να χρειαστούν σημαντικό χρόνο και πόρους για να αναλυθούν, ενώ η χρήση κλιμάκων μιας ερώτησης (μονοδιάστατη) είναι η πιο εύκολη και αποτελεσματική από άποψη χρόνου μέτρα για την αξιολόγηση της έντασης κνησμού που αναφέρθηκε από τον ασθενή στην κλινική πράξη. Η χρήση του 24-h WI-NRS έχει επίσης αναπτυχθεί ως ένα χρήσιμο εργαλείο με μία ερώτηση για την ταχεία αξιολόγηση της σοβαρότητας της φαγούρας. Το WI-NRS αποτελείται από μια επικυρωμένη 11-βαθμολογική κλίμακα που κυμαίνεται από 0 ("χωρίς φαγούρα") έως 10 ("χειρότερη φαγούρα που μπορεί να φανταστεί κανείς") και οι ασθενείς βαθμολογούν την ένταση της χειρότερης φαγούρας τους κατά την προηγούμενη {{15} }h περίοδο [40, 42, 43], με μια 3-βαθμολογική βελτίωση στην κλίμακα επικυρωμένη ως σημαντική βελτίωση [39].
Με βάση τη βαθμολογία WI-NRS και την κατηγορία SADS, ο κνησμός μπορεί να κατηγοριοποιηθεί ως «ήπιος» ή «μέτριος έως σοβαρός» (βαθμολογία WI-NRS Μεγαλύτερη ή ίση με 4, ασθενής SADS τύπου Β ή Γ). Αυτό θα μπορούσε να είναι χρήσιμο για τη σχεδίαση των τροχιών του κνησμού σε μεμονωμένους ασθενείς.

Εκχύλισμα Cistanche
Άλλες κατάλληλες επικυρωμένες μονοδιάστατες κλίμακες για τη μέτρηση της έντασης της φαγούρας που μπορούν να χρησιμοποιηθούν περιλαμβάνουν την οπτική αναλογική κλίμακα (100-mm γραμμή) και την κλίμακα λεκτικής αξιολόγησης (4-βαθμολογική κλίμακα) [40, 42].
Ο αντίκτυπος της φαγούρας στην ποιότητα ζωής του ασθενούς μπορεί επίσης να αξιολογηθεί ρωτώντας τον ασθενή για το πώς η φαγούρα επηρεάζει τον ύπνο ή τη διάθεσή του, μέσω της χρήσης ενός επικυρωμένου μέτρου PRO.
Πολλά διαθέσιμα επικυρωμένα δερματολογικά ερωτηματολόγια PRO μπορούν να χρησιμοποιηθούν για την αξιολόγηση της επίδρασης της φαγούρας στην ποιότητα ζωής (Πίνακας 2), συμπεριλαμβανομένου του Skindex-10 [40], του 5-D itch [44] και του Δείκτη Ποιότητας Ζωής Δερματολογίας [45]. Αυτά τα όργανα χρησιμοποιούνται συχνά στην κλινική έρευνα, αλλά μπορεί να μην είναι τόσο βολικά για χρήση στην κλινική πράξη λόγω του μήκους, της πολυπλοκότητας και του χρόνου που απαιτείται για την ολοκλήρωση και την αξιολόγηση των απαντήσεων.

Τα ερωτηματολόγια μπορεί να μην είναι κατάλληλα για ορισμένους ασθενείς (π.χ. άτομα με σοβαρή οπτική/γνωστική αναπηρία). Αντίθετα, αυτοί οι ασθενείς μπορούν να ερωτηθούν προφορικά για το πώς η φαγούρα επηρεάζει την ποιότητα ζωής τους. Ωστόσο, είναι σημαντικό να αναγνωριστεί ότι τα ερωτηματολόγια μπορεί να μην είναι μια βιώσιμη μέθοδος για την αξιολόγηση της σοβαρότητας της νόσου και της ποιότητας ζωής σε όλους τους ασθενείς. Τα γλωσσικά εμπόδια ή τα εμπόδια γραμματισμού, καθώς και η έλλειψη ενδιαφέροντος των ασθενών για τη συμπλήρωση ερευνών, μπορούν όλα να επηρεάσουν τη χρήση των PRO, αν και αυτό μπορεί να βελτιωθεί με τη χρήση των ePRO [11].
Μεταξύ των θεραπειών για τη θεραπεία των συμπτωμάτων σε ασθενείς σε HD, από ό,τι γνωρίζουμε, το difelikefalin έχει το μεγαλύτερο πρόγραμμα κλινικής ανάπτυξης από οποιονδήποτε αγωνιστή κάπα για CKD-aP σε HD, με 1306 ασθενείς που λαμβάνουν ενεργή θεραπεία σε δοκιμές Φάσης 3, εκ των οποίων 400 έλαβαν τουλάχιστον 1 έτος συνεχούς θεραπείας [13, 46, 47].
Ωστόσο, ήταν οι πρώτες φάσεις του προγράμματος ανάπτυξης φαρμάκων που αποτέλεσαν τη βάση για την μετέπειτα επιτυχία των κλινικών δοκιμών. Ιδιαίτερη σημασία για το difelikefalin ήταν η απόδειξη της έλλειψης μου-αγωνιστικής δράσης ή μεταβολισμού και ο ελάχιστος περιφερικός περιορισμός, με μια μετέπειτα μελέτη αξιολόγησης κατάχρησης που επιβεβαίωσε ότι έχει χαμηλή πιθανότητα ως φάρμακο κατάχρησης [38] και επομένως δεν θεωρείται ελεγχόμενο ουσία [13].
Η αποτελεσματικότητα και η ασφάλεια της ενδοφλέβιας χορήγησης difelikefalin αξιολογήθηκαν με δύο βασικές τυχαιοποιημένες, ελεγχόμενες με εικονικό φάρμακο, δοκιμές Φάσης 3 (KALM-1 και KALM-2) [13, 47, 48], στις οποίες συμμετείχαν συνολικά 851 ενήλικες ασθενείς σε HD με μέτριο έως σοβαρό κνησμό. Σε καθεμία από τις δύο δοκιμές, οι ασθενείς έλαβαν ενδοφλέβια difelikefalin {{1{0}},5 ug/kg ξηρού σωματικού βάρους ή εικονικό φάρμακο μετά από συνεδρίες HD τρεις φορές την εβδομάδα για 12 εβδομάδες. Εκτός από τα κλινικά μέτρα αποτελεσματικότητας, αυτές οι δοκιμές χρησιμοποίησαν επικυρωμένες μετρήσεις PRO της σοβαρότητας της νόσου και της ποιότητας ζωής που σχετίζεται με τον κνησμό, επιτρέποντας την άμεση μέτρηση της βελτίωσης της επιβάρυνσης των συμπτωμάτων CKD-aP σε αυτόν τον συγκεκριμένο πληθυσμό ασθενών. Το ποσοστό των ασθενών που πέτυχαν μεγαλύτερη ή ίση με 3-σημείο μεγαλύτερη μείωση από την αρχική τιμή στις ημερήσιες 24-h βαθμολογίες WI-NRS ήταν σημαντικά μεγαλύτερο με το difelikefalin έναντι του εικονικού φαρμάκου την εβδομάδα 12 (KALM-1 : 49 τοις εκατό έναντι 28 τοις εκατό , P < .001, KALM- 2: 54 τοις εκατό έναντι 42 τοις εκατό , P=.02), καθώς και κάθε εβδομάδα καθ' όλη τη διάρκεια της μελέτης, με σημαντικές βελτιώσεις στον κνησμό -σχετική ποιότητα ζωής, που αναφέρθηκε επίσης στην Εβδομάδα 12 για Skindex-10 και 5-D itch PRO (Εικ. 4) [46, 47]. Η συγκεντρωτική ανάλυση ασφάλειας των KALM-1 και KALM-2 έδειξε ότι οι συχνές ανεπιθύμητες ενέργειες που συμβαίνουν με συχνότητα μεγαλύτερη από ή ίση με 2 τοις εκατό με difelikefalin και μεγαλύτερη από ή ίση με 1 τοις εκατό υψηλότερη από ό, τι στην ομάδα εικονικού φαρμάκου περιελάμβαναν: διάρροια (9,0 τοις εκατό έναντι 5,7 τοις εκατό με εικονικό φάρμακο), ζάλη (6,8 τοις εκατό έναντι 3,8 τοις εκατό), ναυτία (6,6 τοις εκατό έναντι 4,5 τοις εκατό), διαταραχές στη βάδιση, συμπεριλαμβανομένων πτώσεων (6,6 τοις εκατό έναντι 5,4 τοις εκατό) και υπερκαλιαιμία (4,7 τοις εκατό έναντι 3. τοις εκατό ) [49].

Επιπλέον, σε συνδυασμό με τη βελτίωση της σοβαρότητας του κνησμού, η θεραπεία με difelikefalin έχει αποδειχθεί ότι βελτιώνει σημαντικά την ποιότητα του ύπνου σε σύγκριση με το εικονικό φάρμακο (αξιολογήθηκε μέσω του ερωτηματολογίου ποιότητας ύπνου και 5-Ερώτηση αναπηρίας ύπνου σε κλίμακα κνησμού), και τα δύο είναι βασικά επιβαρυντικά συμπτώματα για ασθενείς [8, 50-52].
Στις μελέτες KALM, οι ασθενείς συνέχισαν τυχόν υπάρχοντα φάρμακα κατά της φαγούρας. Αν και περίπου στο ένα τρίτο των ασθενών συνταγογραφήθηκαν ταυτόχρονα φάρμακα κατά του κνησμού, η πλειοψηφία χρησιμοποιούσε αντιισταμινικά, τα οποία είναι απίθανο να είναι αποτελεσματικά στη ΧΝΝ-αΡ, επειδή η ΧΝΝ-αΡ δεν θεωρείται ότι περιλαμβάνει ισταμινεργική οδό [21]. Μόνο στο 1,2 τοις εκατό των ασθενών συνταγογραφήθηκε γκαμπαπεντίνη ως φάρμακο κατά της φαγούρας (αν και σε ορισμένους ασθενείς συνταγογραφήθηκε επίσης γκαμπαπεντίνη για καταστάσεις που δεν σχετίζονται με τη φαγούρα). Ο αλγόριθμος θεραπείας για το CKD-aP (Εικ. 3) προτείνει επομένως την έναρξη θεραπείας με difelikefalin, ως τη μόνη εγκεκριμένη θεραπεία για αυτήν την πάθηση στις ΗΠΑ και την Ευρώπη, καθώς και τη μοναδική θεραπεία με αρκετές κλινικές δοκιμές μεγάλης κλίμακας σε αυτόν τον πληθυσμό ασθενών. Ωστόσο, τα δεδομένα ασφάλειας από τις κλινικές μελέτες έδειξαν ότι οι ασθενείς μπορούν να συνεχίσουν να χορηγούν ταυτόχρονα φάρμακα κατά του κνησμού που έχουν ήδη συνταγογραφηθεί εάν το επιθυμούν.

Εάν οι ασθενείς αντενδείκνυνται για το difelikefalin, δεν είναι διαθέσιμο ή αν αναφέρεται ανθεκτική νόσος, η χρήση της γκαμπαπεντίνης προτείνεται ως εναλλακτική ή επιπρόσθετη θεραπεία, ακολουθούμενη από άλλες θεραπείες, όπως φωτοθεραπεία ή εκλεκτικούς αναστολείς επαναπρόσληψης σεροτονίνης, που έχουν κάποιες ενδείξεις αποτελεσματικότητας σε μικρές, μη ελεγχόμενες κλινικές δοκιμές [53].
ΒΙΒΛΙΟΓΡΑΦΙΚΕΣ ΑΝΑΦΟΡΕΣ
1. Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ. Οδηγίες για τη βιομηχανία: μέτρα έκβασης που αναφέρθηκαν από ασθενείς: χρήση στην ανάπτυξη ιατρικών προϊόντων για την υποστήριξη ισχυρισμών επισήμανσης.
2. Agarwal R. Ανάπτυξη ενός αυτο-χορηγούμενου εργαλείου αξιολόγησης συμπτωμάτων ΧΝΝ. Nephrol Dial Transplant 2010; 25:160– 6.
3. Mittal SK, Ahern L, Flaster E et al. Αυτο-αξιολογημένη σωματική και πνευματική λειτουργία ασθενών που υποβάλλονται σε αιμοκάθαρση. Nephrol Dial Transplant 2001; 16:1387–94.
4. van der Willik EM, Hemmelder MH, Bart HAJ et al. Τακτική μέτρηση της επιβάρυνσης των συμπτωμάτων και της ποιότητας ζωής που σχετίζεται με την υγεία σε ασθενείς που υποβάλλονται σε αιμοκάθαρση: πρώτα αποτελέσματα από το ολλανδικό μητρώο των μετρήσεων έκβασης που αναφέρθηκαν από ασθενείς. Clin Kidney J 2021; 14:1535–44.
5. Lowney AC, Myles ΗΤ, Bristowe Κ, et αϊ. Κατανόηση του τι επηρεάζει την ποιότητα ζωής των ασθενών που υποβάλλονται σε αιμοκάθαρση: μια συλλογική μελέτη στην Αγγλία και την Ιρλανδία. J Pain Symptom Manage 2015;50:778–85.
6. Moskovitch JT, Mount PF, Davies MRP. Οι αλλαγές στην επιβάρυνση των συμπτωμάτων σε ασθενείς που υποβάλλονται σε αιμοκάθαρση αξιολογήθηκαν χρησιμοποιώντας ένα ερωτηματολόγιο αναφοράς συμπτωμάτων στην κλινική. J Palliat Care 2020; 35:59–65.
7. Εκτελεστική Επιτροπή ΤΡΑΓΟΥΔΙΟΥ. Τυποποιημένα αποτελέσματα στη νεφρολογική πρωτοβουλία.
8. Εκτελεστική Επιτροπή ΤΡΑΓΟΥΔΙΟΥ. ΤΡΑΓΟΥΔΙ-HD.
9. Εκτελεστική Επιτροπή ΤΡΑΓΟΥΔΙΟΥ. ΤΡΑΓΟΥΔΙ-Π.Δ.
10. Flythe JE, Hilliard TS, Ikeler K, et al. Προς την καινοτομία με επίκεντρο τον ασθενή: ένα εννοιολογικό πλαίσιο για μέτρα έκβασης που αναφέρονται από ασθενείς για μετασχηματιστικές συσκευές νεφρικής αντικατάστασης. Clin J Am Soc Nephrol 2020; 15:1522–30. https://doi. org/10.2215/cjn.00110120
11. Pérez-Morales R, Buades-Fuster JM, Esteve-Simó V et al. Ηλεκτρονικά αναφερόμενα από τον ασθενή αποτελέσματα στη νεφρολογία: εστίαση στην αιμοκάθαρση. J Clin Med 2022;11:861.
12. Verberne WR, van den Wittenboer ID, Voorend CGN et al. Ποιότητα ζωής που σχετίζεται με την υγεία και συμπτώματα συντηρητικής φροντίδας έναντι αιμοκάθαρσης σε ασθενείς με νεφρική νόσο τελικού σταδίου: μια συστηματική ανασκόπηση. Nephrol Dial Transplant 2021;36:1418–33.
13. Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων. Πληροφορίες συνταγογράφησης Korsuva
14. Shirazian S, Aina O, Park Y et al. Κνησμός που σχετίζεται με χρόνια νεφρική νόσο: επιπτώσεις στην ποιότητα ζωής και τις τρέχουσες προκλήσεις διαχείρισης. Int J Nephrol Renovasc Dis 2017; 10:11–26.
15. Sukul Ν, Karaboyas Α, Csomor PA et αϊ. Αυτοαναφερόμενος κνησμός και κλινικά, σχετιζόμενα με την αιμοκάθαρση και αποτελέσματα που αναφέρθηκαν από τον ασθενή σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. Kidney Med 2021; 3: 42–53.
16. Nowak DA, Yeung J. Διάγνωση και θεραπεία κνησμού. Can Fam Physician 2017; 63:918–24
17. Rayner HC, Larkina Μ, Wang Μ, et αϊ. Διεθνείς συγκρίσεις επιπολασμού, ευαισθητοποίησης και θεραπείας του κνησμού σε άτομα που υποβάλλονται σε αιμοκάθαρση. Clin J Am Soc Nephrol 2017; 12:2000– 7.
18. Pisoni RL, Wikström B, Elder SJ et al. Κνησμός σε ασθενείς που υποβάλλονται σε αιμοκάθαρση: διεθνή αποτελέσματα από τη μελέτη Dialysis Outcomes and Practice Patterns Study (DOPPS). Nephrol Dial Transplant 2006;21:3495–505.
19. Weiss Μ, Mettang Τ, Tschulena U et al. Ποιότητα ζωής που σχετίζεται με την υγεία σε ασθενείς που υποβάλλονται σε αιμοκάθαρση που υποφέρουν από χρόνιο κνησμό: αποτελέσματα από το GEHIS (Γερμανική Επιδημιολογία Αιμοκάθαρσης Μελέτη φαγούρας). Qual Life Res 2016; 25:3097–106.
20. Ahdoot RS, Kalantar-Zadeh K, Burton JO, et al. Μια νέα προσέγγιση σε ομάδες δυσάρεστων συμπτωμάτων που περιβάλλουν τον κνησμό σε ασθενείς με χρόνια νεφρική νόσο και σε θεραπεία αιμοκάθαρσης. Curr Opin Nephrol Hypertens 2022; 31:63–71
21. Reddy VB, Iuga AO, Shimada SG et al. Η φαγούρα που προκαλείται από το Cowhage προκαλείται από μια νέα πρωτεάση κυστεΐνης: ένας συνδέτης υποδοχέων που ενεργοποιούνται από πρωτεάση. J Neurosci 2008; 28:4331–5.
22. Lanot A, Kottler D, Béchade C. [Χρόνια νεφρική νόσος που σχετίζεται με κνησμό]. Nephrol Ther 2021; 17:488–95.
23. Verduzco HA, Shirazian S. σχετιζόμενος με CKD κνησμός: νέες γνώσεις για τη διάγνωση, την παθογένεια και τη διαχείριση. Kidney Int Rep 2020; 5:1387–402.
24. Namer B, Carr R, Johanek LM et al. Ξεχωριστές περιφερειακές οδούς για κνησμό στον άνθρωπο. J Neurophysiol 2008; 100:2062-9.
25. Aquino TMO, Luchangco KAC, Sanchez EV et al. Μια τυχαιοποιημένη ελεγχόμενη μελέτη τοπικού σκευάσματος γκαμπαπεντίνης 6 τοις εκατό για κνησμό που σχετίζεται με χρόνια νεφρική νόσο. Int J Dermatol 2020; 59:955–61.
26. Agarwal P, Garg V, Karagaiah P, et al. Κνησμός που σχετίζεται με χρόνια νεφρική νόσο. Toxins 2021; 13:527.
27. Shirazian S, Aina O, Park Y et al. Κνησμός που σχετίζεται με χρόνια νεφρική νόσο: επιπτώσεις στην ποιότητα ζωής και τις τρέχουσες προκλήσεις διαχείρισης. Int J Nephrol Renovasc Dis 2017; 10:11–26.
28. Mettang T, Kremer AE. Ουραιμικός κνησμός. Kidney Int 2015; 87:685–91.
29. Wieczorek A, Krajewski P, Kozioł-Gałczy ´nska M et al. Έκφραση υποδοχέων οπιοειδών στο δέρμα ασθενών που υποβάλλονται σε αιμοκάθαρση που πάσχουν από ουραιμικό κνησμό. J Eur Acad Dermatol Venereol 2020; 34:2368–72.
30. Legroux-Crespel E, Clèdes J, Misery L. Συγκριτική μελέτη για τις επιδράσεις της ναλτρεξόνης και της λοραταδίνης στον ουραιμικό κνησμό. Dermatology 2004; 208:326–30.
31. Pauli-Magnus C, Mikus G, Alscher DM et al. Η ναλτρεξόνη δεν ανακουφίζει από τον ουραιμικό κνησμό: αποτελέσματα μιας τυχαιοποιημένης, διπλής-τυφλής, ελεγχόμενης με εικονικό φάρμακο διασταυρούμενης μελέτης. J Am Soc Nephrol 2000; 11:514–9.
32. Peer G, Kivity S, Agami O et al. Τυχαιοποιημένη διασταυρούμενη δοκιμή ναλτρεξόνης σε ουραιμικό κνησμό. Lancet 1996;348:1552–4.
33. Kumagai Η, Ebata T, Takamori K et al. Επίδραση ενός νέου αγωνιστή υποδοχέα κάπα, υδροχλωρικής ναλφουραφίνης, σε σοβαρή φαγούρα σε 337 ασθενείς που υποβάλλονται σε αιμοκάθαρση: μια φάση ΙΙΙ, τυχαιοποιημένη, διπλά-τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη. Nephrol Dial Transplant 2010;25:1251–7.
34. Mathur VS, Kumar J, Crawford PW, et al. Μια πολυκεντρική, τυχαιοποιημένη, διπλά-τυφλή, ελεγχόμενη με εικονικό φάρμακο δοκιμή δισκίων ναλβουφίνης ER για ουραιμικό κνησμό. Am J Nephrol 2017; 46:450–8.
35. Σύνοψη Ηλεκτρονικών Φαρμάκων. Περίληψη των χαρακτηριστικών του προϊόντος Kapruvia.
36. Kardon AP, Polgár Ε, Hachisuka J et al. Η Dynorphin δρα ως νευροδιαμορφωτής για την αναστολή της φαγούρας στο ραχιαίο κέρας του νωτιαίου μυελού. Neuron 2014; 82:573-86.
37. Cowan A, Kehner GB, Inan S. Targeting itch with ligands selective for k opioid receptors. Handb Exp Pharmacol 2015;226:291–314.
38. Shram MJ, Spencer RH, Qian J, et αϊ. Αξιολόγηση της δυνατότητας κατάχρησης της difelikefalin, ενός εκλεκτικού αγωνιστή υποδοχέα κάπα-οπιοειδών, σε ψυχαγωγικούς χρήστες πολλαπλών ναρκωτικών. Clin Transl Sci 2022; 15:535–47.
39. Vernon MK, Swett LL, Speck RM et αϊ. Ψυχομετρική επικύρωση και κατώφλια ουσιαστικής αλλαγής της Κλίμακας Αριθμητικής Βαθμολόγησης Χειρότερης Έντασης Κνησμού για την αξιολόγηση του κνησμού σε ασθενείς με κνησμό που σχετίζεται με χρόνια νεφρική νόσο. J Patient Rep Outcomes 2021;5:134.
40. Mathur VS, Lindberg J, Germain Μ, et al. Μια διαχρονική μελέτη του ουραιμικού κνησμού σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. Clin J Am Soc Nephrol 2010; 5:1410–9.
41. Manenti L, Leuci E. Αισθάνεστε φαγούρα; Ένας οδηγός για τη διάγνωση και τη μέτρηση του κνησμού που σχετίζεται με τη χρόνια νεφρική νόσο σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. Clin Kidney J 2021;14:i8–15.
42. Phan NQ, Blome C, Fritz F et al. Εκτίμηση της έντασης του κνησμού: μια προοπτική μελέτη για την εγκυρότητα και την αξιοπιστία της οπτικής αναλογικής κλίμακας, της κλίμακας αριθμητικής βαθμολογίας και της κλίμακας λεκτικής βαθμολογίας σε 471 ασθενείς με χρόνιο κνησμό. Acta Derm Venereol 2012; 92:502–7.
43. Vernon M, Ständer S, Munera C et al. Κλινικά σημαντική αλλαγή στις βαθμολογίες έντασης κνησμού: αξιολόγηση σε ασθενείς με κνησμό που σχετίζεται με χρόνια νεφρική νόσο. J Am Acad Dermatol 2021;84:1132–4.
44. Elman S, Hynan LS, Gabriel V et al. Η κλίμακα 5-D φαγούρα: μια νέα μέτρηση του κνησμού. Br J Dermatol 2010; 162:587–93.
45. Basra MK, Fenech R, Gatt RM et αϊ. Ο Δείκτης Ποιότητας Ζωής Δερματολογίας 1994-2007: μια ολοκληρωμένη ανασκόπηση των δεδομένων επικύρωσης και των κλινικών αποτελεσμάτων. Br J Dermatol 2008; 159:997-1035.
46. Fishbane S, Wen W, Munera C, et αϊ. Μακροπρόθεσμη ασφάλεια και αποτελεσματικότητα του difelikefalin σε ασθενείς με κνησμό που σχετίζεται με χρόνια νεφρική νόσο: ανάλυση από το KALM-1 και το KALM-2. Am J Kidney Dis 2021; 77:593–4.
47. Wooldridge TD, Mccafferty Κ, Schoemig Μ et al. Αποτελεσματικότητα και ασφάλεια του difelikefalin για μέτριο έως σοβαρό κνησμό που σχετίζεται με ΧΝΝ: μια παγκόσμια μελέτη φάσης 3 σε ασθενείς που υποβάλλονται σε αιμοκάθαρση (KALM-2). J Am Soc Nephrol 2020; 31:22–3.
48. Fishbane S, Jamal Α, Munera C, et αϊ. Μια δοκιμή φάσης 3 της difelikefalin σε ασθενείς που υποβάλλονται σε αιμοκάθαρση με κνησμό. N Engl J Med 2019;382:222–32.
49. Cara Therapeutics Inc. KORSUVA (difelikefalin) ένεση για ενδοφλέβια χρήση. Κύρια σημεία των πληροφοριών συνταγογράφησης.
50. Ahdoot RS, Kalantar-Zadeh K, McCafferty K et al. Βελτίωση της ποιότητας του ύπνου από τη μείωση της έντασης του κνησμού σε ασθενείς με μέτριο έως σοβαρό κνησμό που υποβάλλονται σε αιμοκάθαρση. Παγκόσμιο Συνέδριο για την φαγούρα. Εικονική 2021.
51. Weiner DE, Walpen S, Schaufler Τ et al. Η μείωση του κνησμού με difelikefalin συσχετίζεται με βελτιωμένη ποιότητα ύπνου σε ασθενείς που υποβάλλονται σε αιμοκάθαρση με κνησμό. American Society of Nephrology 2021 Virtual, 2021;
52. Fishbane S, Mathur V, Germain MJ et al. Τυχαιοποιημένη ελεγχόμενη δοκιμή της difelikefalin για χρόνιο κνησμό σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. Kidney Int Rep 2020; 5:600–10.
53. Lipman ZM, Paramasivam V, Yosipovitch G et al. Κλινική διαχείριση του κνησμού που σχετίζεται με χρόνια νεφρική νόσο: τρέχουσες θεραπευτικές επιλογές και μελλοντικές προσεγγίσεις. Clin Kidney J 2021;14:i16–22.
54. Jhamb Μ, Weisbord SD, Steel JL et al. Κόπωση σε ασθενείς που υποβάλλονται σε αιμοκάθαρση συντήρησης: ανασκόπηση ορισμών, μέτρων και παραγόντων που συμβάλλουν. Am J Kidney Dis 2008; 52:353-65.
55. Nadort Ε, Schouten RW, Witte SHS et al. Θεραπεία των τρεχόντων καταθλιπτικών συμπτωμάτων σε ασθενείς που υποβάλλονται σε αιμοκάθαρση: μια συστηματική ανασκόπηση και μετα-ανάλυση. Gen Hosp Psychiatry 2020; 67: 26–34.
56. Raina R, Krishnappa V, Gupta M. Διαχείριση του πόνου σε ασθενείς με νεφρική νόσο τελικού σταδίου: μια σύντομη ανασκόπηση. Hemodial Int 2018; 22:290–6.
57. Ishida JH, McCulloch CE, Steinman ΜΑ, et al. Χρήση γκαμπαπεντίνης και πρεγκαμπαλίνης και συσχέτιση με ανεπιθύμητες εκβάσεις σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. J Am Soc Nephrol 2018; 29:1970–8.
58. Davison SN. Ο επιπολασμός και η διαχείριση του χρόνιου πόνου σε νεφρική νόσο τελικού σταδίου. J Palliat Med 2007, 10:1277–87.
59. Cohen SD, Cukor D, Kimmel PL. Άγχος σε ασθενείς που υποβάλλονται σε θεραπεία με αιμοκάθαρση. Clin J Am Soc Nephrol 2016; 11:2250–5.
60. Μουτζάις Σ.Κ. Μυϊκές κράμπες κατά την αιμοκάθαρση. Int J Artif Organs 1994; 17:570–2.
61. Lynch KE, Feldman ΗΙ, Berlin JA et al. Επιδράσεις της L-καρνιτίνης στην υπόταση που σχετίζεται με την αιμοκάθαρση και τις μυϊκές κράμπες: μια μετα-ανάλυση. Am J Kidney Dis 2008; 52:962–71.
62. Salib Μ, Memon ΑΝ, Gowda AS et al. Ασθενείς με αιμοκάθαρση με σύνδρομο ανήσυχων ποδιών: μπορούμε να ανακουφίσουμε την ταλαιπωρία τους; Cureus 2020; 12:e10053.
63. O'Connor NR, Corcoran AM. Νεφρική νόσος τελικού σταδίου: διαχείριση συμπτωμάτων και σχεδιασμός εκ των προτέρων φροντίδας. Am Fam Physician 2012; 85:705–10.
64. Novak Μ, Shapiro CM, Mendelssohn D et al. Διάγνωση και αντιμετώπιση της αϋπνίας σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. Semin Dial 2006; 19:25–31.
65. Mathur VS, Lindberg J, Germain Μ et al.Investigators INR. Μια διαχρονική μελέτη του ουραιμικού κνησμού σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. Clin J Am Soc Nephrol 2010; 5:1410–9.
Rajiv Agarwal 1, James Burton 2, Maurizio Gallieni 3, Kamyar Kalantar-Zadeh 4, Gert Mayer 5, Carol Pollock 6 και Jacek C. Szepietowski 7.
1 Ρίτσαρντ Λ. Ρούντεμπους VA Ιατρική Κέντρο και Ιντιάνα Πανεπιστήμιο, Ινδιανάπολη, IN, ΗΠΑ%2γ
2 Τμήμα Καρδιαγγειακών Επιστημών, Πανεπιστημιακά Νοσοκομεία Leicester NHS Trust, Leicester, UK,
3 Τμήμα Βιοϊατρικών και Κλινικών Επιστημών «Luigi Sacco», Università Di Milano, Milano, Italy,
4 Τμήμα Νεφρολογίας, Υπέρτασης και Μεταμόσχευσης Νεφρού, Πανεπιστήμιο της Καλιφόρνια, Irvine, CA, ΗΠΑ,
5 Τμήμα Εσωτερικής Ιατρικής IV (Νεφρολογία και Υπέρταση), Ιατρικό Πανεπιστήμιο Innsbruck, Innsbruck, Αυστρία,
6 Εργαστήριο Νεφρικής Έρευνας, Ινστιτούτο Kolling, Πανεπιστήμιο του Σίδνεϊ, Royal North Shore Hospital, St Leonards, Σίδνεϊ, Αυστραλία.
7 Τμήμα Δερματολογίας, Αφροδισιολογίας και Αλλεργιολογίας, Ιατρικό Πανεπιστήμιο, Βρότσλαβ, Πολωνία.






