Μια διακριτική κατανομή του επαγόμενου από υποξία παράγοντα-1 σε καλλιεργημένα νεφρικά σωληναριακά κύτταρα με προσομοίωση υποαιμάτωσης με τοποθέτηση καλυπτρίδας
Mar 27, 2022
Επικοινωνία: Audrey Hu Whatsapp/hp: 0086 13880143964 Email:audrey.hu@wecistanche.com
Tomoko Honda1| Yosuke Hirakawa1 | Kiichi Mizukami2| Toshitada Yoshihara2| Τετσουχίρο Τανάκα1| Seiji Tobita2| Μασαόμι Νανγκάκου
Αφηρημένη
Η χρόνια υποξία στο διάμεσο νεφρικό σωληνάριο παίζει βασικό ρόλο στην εξέλιξη της χρόνιαςνεφρόνόσος(ΧΝΝ). Ως εκ τούτου, είναι σημαντικό να διερευνηθεί η σωληναριακή υποξία και η δραστηριότητα του επαγόμενου από την υποξία παράγοντα (HIF)-1 ως απόκριση στην υποξία. Η αραίωση του περισωληναρίου τριχοειδούς προκαλεί υποαιμάτωση στη ΧΝΝ. Ωστόσο, η επίδραση της υποαιμάτωσης στα HIF έχει σπάνια διερευνηθεί. Προκαλέσαμε υποαιμάτωση που προκαλείται από την τοποθέτηση καλυπτρίδας στον άνθρωπονεφρό-2 κύτταρα και παρατήρησαν μια κλίση οξυγόνου κάτω από την καλυπτρίδα. Η ανοσοκυτταροχημεία του HIF-1 έδειξε έναν σχηματισμό σε σχήμα ντόνατς στην άκρη μιας θετικής στην πιμονιδαζόλη περιοχής, την οποία ονομάσαμε "HIF-ring". Η τάση οξυγόνου του δακτυλίου HIF εκτιμήθηκε ότι είναι μεταξύ περίπου 4 mmHg και 20 mmHg. Αυτό το αποτέλεσμα δεν ήταν συμβατό με εκείνα προηγούμενης έρευνας που έδειχνε συσσώρευση HIF-1 στο ανοξικό εύρος με ομοιογενή τάση οξυγόνου. Παρατηρήσαμε περαιτέρω την παρουσία μιας διαβάθμισης pH κάτω από μια καλυπτρίδα, καθώς και μια μετατόπιση του δακτυλίου HIF λόγω αλλαγών στο pH του μέσου καλλιέργειας, υποδηλώνοντας ότι ο δακτύλιος HIF σχηματίστηκε από την καταστολή του HIF-1 που σχετίζεται με σε χαμηλό pH. Αυτή η έρευνα έδειξε ότι η ενεργοποίηση του HIF{10}} μιμείται τη φυσιολογική κατάσταση σε καλλιεργημένα κύτταρα με υποαιμάτωση.
ΛΕΞΕΙΣ ΚΛΕΙΔΙΑυποαιμάτωση, υποξία, παράγοντας που προκαλείται από υποξία, βαθμίδα οξυγόνου, pH
Cistanche herbaαποτρέπει την νεφρική νόσο, κάντε κλικ εδώ για να λάβετε το δείγμα
1|ΕΙΣΑΓΩΓΗ
Η επίπτωση της χρόνιαςνεφρόνόσος(ΧΝΝ) αυξάνεται σε όλο τον κόσμο καθώς οι κοινωνίες γερνούν (Tonelli & Riella, 2014). Η εξέλιξη της ΧΝΝ είναι μη αναστρέψιμη όταν η νεφρική βλάβη φτάσει σε κάποιο βαθμό και τελικά καταλήγει σε νεφρική νόσο τελικού σταδίου (ESRD), ανεξάρτητα από την υποκείμενη νόσο. Αυτό το αποτέλεσμα υποδηλώνει την ύπαρξη μιας «τελικής κοινής οδού». Σύμφωνα με προηγούμενες παθολογικές αναλύσεις, η μείωση της νεφρικής λειτουργίας συσχετίζεται ισχυρότερα με τη σωληναριδική βλάβη παρά με τη σπειραματική βλάβη. Έχουν υπάρξει αρκετές αναφορές που καταδεικνύουν ότι η νεφρική ίνωση προκαλεί χρόνια υποξία στο διάμεσο του σωληναρίου και αυτή η σωληναρισιακή υποξία επιδεινώνει τη ΧΝΝ και οδηγεί σε ESRD. Αυτά τα στοιχεία υποδεικνύουν ότι η σωληνοειδής διάμεση υποξία παίζει ρόλο στην τελική κοινή οδό της ΧΝΝ (Mimura & Nangaku, 2010; Nangaku, 2006). ονεφρόείναι πολύ ευαίσθητο στην υποξία λόγω της υψηλής ζήτησης για οξυγόνο και της ύπαρξης διακλάδωσης οξυγόνου μεταξύ των ενδονεφρικών αρτηριών και φλεβών (Nangaku, 2006; Welch et al., 2001; Zhang et al., 2014). Ως εκ τούτου, θεωρούμε ότι είναι απαραίτητο να διερευνηθεί η υποξία και η ανταπόκριση στην υποξία στο νεφρικό σωληνάριο διάμεσο.
Η πρωταρχική βιολογική απόκριση στην υποξία σε ζωντανούς οργανισμούς λαμβάνει χώρα μέσω της οδού του επαγόμενου από την υποξία παράγοντα (HIF) (Hypoxia, 2011; Semenza & Wang, 1992; Zhou et al., 2003). Το HIF αποτελείται από - και - υπομονάδες. Αν και η -υπομονάδα είναι συστατικά ενεργή, η -υπομονάδα αποικοδομείται παρουσία οξυγόνου. Υπό νορμοξικές συνθήκες, το HIF- υδροξυλιώνεται από τον τομέα της προλυλ υδροξυλάσης (Ph.D.), καθιστώντας τον αναγνωρίσιμο από τον καταστολέα όγκου von Hippel–Lindau (VHL). Αυτή η αναγνώριση έχει ως αποτέλεσμα την ουβικουιτίνη και την αποικοδόμηση του υδροξυλιωμένου HIF- στο πρωτεάσωμα. Σε συνθήκες υποξίας, το HIF- συσσωρεύεται στο κυτταρόπλασμα, επειδή το μη υδροξυλιωμένο HIF- διαφεύγει της αποικοδόμησης. Το συσσωρευμένο HIF- μετατοπίζεται από το κυτταρόπλασμα στον πυρήνα, όπου διμερίζεται με το HIF- και δρα ως μεταγραφικός παράγοντας, προάγοντας την έκφραση των κατάντη γονιδίων. Από τις τρεις ταυτοποιημένες ισομορφές των υπομονάδων HIF—HIF-1, HIF{-2 και HIF{-3—τα επιθηλιακά κύτταρα των νεφρικών σωληναρίων είναι γνωστό ότι εκφράζουν HIF-1 (Tanaka et al ., 2016). Προηγούμενες μελέτες έχουν δείξει παροδική ή περιφερειακή συσσώρευση HIF στονεφρόμε ΧΝΝ (Goldfarb et al., 2006; Yu et al., 2012) και αυτό το HIF ενεργοποιείται στη μειωμένη τάση οξυγόνου στο περιβάλλον ΧΝΝ. Η κακή προσαρμογή στην υποξία στη ΧΝΝ μπορεί να προκαλείται από την παρουσία παραγόντων που καταστέλλουν τις οδούς HIF (Asai et al., 2016; Tanaka et al., 2013; Thangarajah et al., 2009). Προστατευτικές επιδράσεις της ενεργοποίησης του HIF έχουν αναφερθεί σε πολλά ζωικά μοντέλα, συμπεριλαμβανομένων των διαβητικών αρουραίων που προκαλούνται από στρεπτοζοτοκίνη και των αρουραίων με νεφρεκτομή 5/6 (Deng et al., 2010; Nordquist et al., 2015). Ph.D. Οι αναστολείς έχουν προσελκύσει πρόσφατα την προσοχή ως νέες θεραπευτικές προσεγγίσεις για τη νεφρική αναιμία σε ασθενείς με ΧΝΝ (Akizawa et al., 2019; Chen et al., 2017, 2019; Coyne et al., 2017; Miyata et al., 2011; Pergola et al., 2019 ., 2016· Provenzano et al., 2016). Ωστόσο, οι λεπτομέρειες της εξέλιξης της νεφρικής υποξίας και ο τρόπος με τον οποίο εμφανίζεται η συσσώρευση HIF στονεφρόμε ΧΝΝ, παραμένουν ασαφείς. Η εξαρτώμενη από το οξυγόνο υδροξυλίωση του HIF- λαμβάνει χώρα στο κυτταρόπλασμα, και επομένως είναι σημαντικό να μετρηθεί η ενδοκυτταρική και εξωκυτταρική τάση οξυγόνου. Υπάρχουν διάφορες μέθοδοι που χρησιμοποιούνται για τη μέτρηση της τάσης οξυγόνου, συμπεριλαμβανομένης της χρήσης μικροηλεκτροδίων ή απεικόνισης μαγνητικού συντονισμού που εξαρτάται από το επίπεδο οξυγόνου του αίματος (BOLD-MRI). Χρησιμοποιήσαμε μικροσκοπία απεικόνισης εφ' όρου ζωής φωσφορισμού (PLIM) για ποσοτική μέτρηση της κατάστασης του ενδοκυτταρικού οξυγόνου (Hirakawa et al., 2017; Yoshihara et al., 2015). Το BTPDM1 είναι μια φωσφορίζουσα χρωστική ουσία που βασίζεται στο σύμπλοκο ιριδίου (III) BTP, (bp)2Ir(acc) (bp=βενζοϊκή-πυριδίνη, aac=ακετυλακετόνη) με μια κατιονική διμεθυλαμινο ομάδα, η οποία είναι παθητικά κατανέμεται σε ενδοκυτταρικά λυσοσώματα. Συντέθηκε ως φωσφοπρόσφατος ανιχνευτής για τη μέτρηση της ενδοκυτταρικής πίεσης οξυγόνου (Yoshihara et al., 2015). Το PLIM με BTPDM1 επέτρεψε τη λήψη εικόνων υψηλής ανάλυσης της μερικής πίεσης του οξυγόνου σε νεφρικά σωληναριακά κύτταρα στη νεφρική επιφάνεια φυσιολογικών ποντικών, παρέχοντας δεδομένα που υποδεικνύουν την παρουσία βαθμίδας οξυγόνου, ακόμη και σε φυσιολογικούς νεφρούς (Hirakawa et al., 2018 ).
Υπάρχουν βαθμίδες οξυγόνου σε ζωντανά όργανα, συμπεριλαμβανομένωννεφρά, ακόμη και υπό κανονικές συνθήκες (Hirakawa et al., 2018; Kietzmann, 2017; Zhdanov et al., 2015), και επομένως τέτοιες διαβαθμίσεις μπορούν επίσης να αναμένονται στη ΧΝΝ. Η υποαιμάτωση προκαλείται από την αραίωση του μικροαγγειακού συστήματος στη ΧΝΝ, στην οποία η προοδευτική σπειραματική βλάβη έχει ως αποτέλεσμα τη μείωση της περισωληνιακής τριχοειδούς ροής αίματος, επιδεινώνοντας τη διάμεση ίνωση. Η διάμεση ίνωση βλάπτει τη διάχυση και την παροχή οξυγόνου στα σωληναριακά κύτταρα και οδηγεί στη σπανίωση του μικροαγγειακού συστήματος, επιδεινώνοντας περαιτέρω τη σωληναριδική υποξία (Mimura & Nangaku, 2010; Nangaku, 2006). Οι βιολογικές επιδράσεις της υποαιμάτωσης, ωστόσο, παραμένουν ασαφείς, επειδή οι περισσότερες μελέτες έχουν διερευνήσει τις επιδράσεις της υποξίας και του HIF-1 σε καλλιεργημένα κύτταρα υπό συνθήκες ομοιογενούς αιμάτωσης και τάσης οξυγόνου (Rexius-Hall et al., 2017). Προηγούμενες μελέτες έχουν δείξει ότι τα μονοστιβαδικά καλλιεργημένα κύτταρα που καλύπτονται με καλυπτρίδα παρέχουν ένα καλό μοντέλο υποδιάχυσης που προκαλείται από ένα φραγμό στη διάχυση στο μέσο καλλιέργειας. Η μοντελοποιημένη υποαιμάτωση σχετίζεται με μια βαθμίδα οξυγόνου επειδή μια καλυπτρίδα εμποδίζει τη διάχυση οξυγόνου από την κορυφή του μέσου στα κύτταρα (Pitts & Toombs, 2004; Takahashi & Sato, 2010; Yoshihara et al., 2015). Σε μια μονοστιβάδα καλλιεργημένων κυττάρων που καλύπτονται με καλυπτρίδα, η ενδοκυτταρική τάση οξυγόνου πέφτει με την απόσταση από το άκρο της καλυπτρίδας λόγω περιορισμένης διάχυσης οξυγόνου στα καλλιεργημένα κύτταρα. Ως αποτέλεσμα, σχηματίζεται μια βαθμίδα οξυγόνου από την άκρη προς το κέντρο της καλυπτρίδας και η ενδοκυτταρική τάση οξυγόνου μπορεί να πέσει σε μια ανοξική περιοχή στο κέντρο της καλυπτρίδας (Takahashi & Sato, 2010; Yoshihara et al., 2015) . Στην τρέχουσα μελέτη, εστιάσαμε στην ενεργοποίηση του HIF και διερευνήσαμε εάν υπάρχει μια ανεξάρτητη από το οξυγόνο αλλαγή στην έκφραση του HIF παρουσία υποαιμάτωσης με βαθμίδα οξυγόνου. Δεδομένου ότι η υποαιμάτωση με βαθμίδα οξυγόνου υπάρχει στα νεφρικά σωληνάρια in vivo, η παρατήρηση ανεξάρτητων από οξυγόνο επιδράσεων στην έκφραση του HIF στο μοντέλο καλυπτρίδας μπορεί να παρέχει πληροφορίες για τον μηχανισμό που κρύβεται πίσω από την ανεπάρκεια της συσσώρευσης HIF στη ΧΝΝ.

εκχύλισμα κιστάνιγια νεφρό
2|ΥΛΙΚΑ ΚΑΙ ΜΕΘΟΔΟΙ
2.1|Κυτταρικής καλλιέργειας
Τα καλλιεργημένα κύτταρα επωάστηκαν σε έναν υγροποιημένο επωαστήρα με 5 τοις εκατό CO2. Η υποξική επώαση πραγματοποιήθηκε σε έναν προσωπικό επωαστήρα CO2/πολλαπλών αερίων APM-30D (Astec). Η ανοξία προκλήθηκε με σάκο ανοξίας, AnaeroPack και σετ Αναερόβιας καλλιέργειας #Α-13 (Mitsubishi Gas Chemical).
Κύτταρα HK-2 (Homo sapiens, άνθρωποςνεφρό, αρσενικό, CRL- 2190, ATCC, RRID: CVCL_0302), μια απαθανατισμένη επιθηλιακή κυτταρική σειρά εγγύς σωληναρίου από φυσιολογικό ανθρώπινο νεφρό ενηλίκου, καλλιεργήθηκαν στο τροποποιημένο μείγμα θρεπτικών ουσιών της Dulbecco's Eagle F{{2} } Ζαμπόν (DMEM/F12) (D8062, Sigma Aldrich) που περιέχει 10 τοις εκατό εμβρυϊκό βόειο ορό (FBS) (F7524, Sigma Aldrich) και διάλυμα πενικιλλίνης-στρεπτομυκίνης (15070063, Thermo Fisher Scientific) σε ένα δίσκο καλλιέργειας 10 cm. Για το πέρασμα, τα κύτταρα HK{10}} διαχωρίστηκαν με θρυψίνη (204-16935, Wako Pure Chemical Industries, Ltd.) και φυγοκεντρήθηκαν στα 300 g για 5 λεπτά.
HeLa καρκινικά κύτταρα τραχήλου της μήτρας και ανθρώπινο εμβρυϊκόνεφρόΤα κύτταρα 293 (ΗΕΚ293) καλλιεργήθηκαν σε DMEM με χαμηλή (1000 mg/L) γλυκόζη (D6046, Sigma Aldrich) που περιείχε 5 τοις εκατό FBS σε ένα τρυβλίο καλλιέργειας 10 cm. Αυτά τα κύτταρα διαβιβάστηκαν ως κύτταρα HK-2.
Επιθηλιακά κύτταρα εγγύς νεφρικού σωληναρίου (RPTECs) (CC- 2553, Cambrex) διατηρήθηκαν χρησιμοποιώντας κιτ RenaLifeTM Comp (LRC-LL0025, Lonza Ltd.). Για το πέρασμα, τα RPTEC διαχωρίστηκαν χρησιμοποιώντας θρυψίνη, εξουδετερώθηκαν με διάλυμα εξουδετέρωσης τρυψίνης (CC-5002, Lonza Ltd.) και φυγοκεντρήθηκαν στα 200 g για 5 λεπτά.
2.2|Καθιέρωση μοντέλου υποαιμάτωσης με τοποθέτηση καλυπτρίδας
Στρογγυλού σχήματος καλυπτρίδες διαμέτρου 15 mm (C015001, Matsunami) καθαρίστηκαν με χρήση υπερήχων και αποθηκεύτηκαν σε αιθανόλη 99,5 τοις εκατό πριν από τη χρήση. Χρησιμοποιήθηκαν δύο μέθοδοι, βασισμένες στην παρατήρηση κυττάρων έξω από την καλυπτρίδα.
Μονοστοιβάδες καλλιεργημένα κύτταρα τοποθετήθηκαν μεταξύ μιας καλυπτρίδας και του πυθμένα ενός τρυβλίου (Σχήμα S1a,b) ή μιας εναλλακτικής μεθόδου (Εικόνα S1c), όπως περιγράφεται παρακάτω. Είτε η παραδοσιακή είτε η εναλλακτική μέθοδος επιλέχθηκε για να καθιερωθεί το μοντέλο μας καλυπτρίδας για ζωντανή απεικόνιση, είτε απεικόνιση οξυγόνου είτε απεικόνιση PH. Για την ανοσοκυτταροχημεία (ICC), επιλέχθηκε η εναλλακτική μέθοδος, επειδή κατά τη χρήση της παραδοσιακής μεθόδου, η πλειονότητα των κυττάρων αποσπάται συχνά από τον πυθμένα του πιάτου κατά την αφαίρεση της καλυπτρίδας για στερέωση κυττάρων (Εικόνα S2a).
2.2.1|Παραδοσιακή μέθοδος
Την Ημέρα 1, τα κύτταρα τοποθετήθηκαν στον πυθμένα ενός γυάλινου δίσκου 27 mm (3910-035, Iwaki) σε μια συμβολή 100 τοις εκατό * (περίπου 5,0 × 105/πιάτο). Καλλιεργήθηκαν σε DMEM/F12 που περιείχε 10 τοις εκατό FBS χωρίς αντιβιοτικό κατά τη διάρκεια της νύχτας. Την Ημέρα 2, τοποθετήθηκε μια καλυπτρίδα πάνω από τα καλλιεργημένα κύτταρα για την περίοδο που υποδεικνύεται (Εικόνα S1b).
2.2.2|Εναλλακτική μέθοδος
Τα κύτταρα σπάρθηκαν σε καλυπτρίδα σε τρυβλίο καλλιέργειας 35 mm σε συρροή 1{4}}0 τοις εκατό (περίπου 5,0 × 105/τρυβλίο) την Ημέρα.
1. Καλλιεργήθηκαν σε DMEM/F12 που περιείχε 10 τοις εκατό FBS χωρίς διάλυμα αντιβιοτικού όλη τη νύχτα. Την Ημέρα 2, η ολίσθηση κάλυψης αναστράφηκε, για να προσαρτηθεί η επιφάνεια των κυψελών της στον πυθμένα ενός νέου γυάλινου δίσκου 27 mm για μια καθορισμένη περίοδο (Εικόνα S1c).
Δημιουργήσαμε επίσης ένα μοντέλο καλυπτρίδας χρησιμοποιώντας καλυπτρίδες στρογγυλού σχήματος με διάμετρο 10 mm (CS01005, Matsunami) (Εικόνα S2b).
2.3|Απεικόνιση ζωντανού οξυγόνου με BTPDM1
Τα καλλιεργημένα κύτταρα παρασκευάστηκαν την Ημέρα 1, όπως περιγράφεται παραπάνω. Την ημέρα 2, τα κύτταρα ξεπλύθηκαν δύο φορές με διάλυμα Hanks' Balanced Salt (HBSS) (H8264, Sigma Aldrich) και επωάστηκαν με 500 nM BTPDM1, μια κατιονική λιπόφιλη χρωστική ουσία με βάση το ιρίδιο που χρησιμοποιείται ως ενδοκυτταρικός φωσφορίζων ανιχνευτής (Al.Yoshihar, 2015), σε DMEM/F12 χωρίς ερυθρό φαινόλης (21041-025, Thermo Fisher Scientific) για 30 λεπτά. Αφού τα κύτταρα πλύθηκαν δύο φορές με HBSS, τοποθετήθηκαν μεταξύ μιας καλυπτρίδας και του πυθμένα ενός πιάτου, όπως περιγράφεται παραπάνω. Η ένταση του φωσφορισμού από το BTPDM1 σε καλλιεργημένα κύτταρα καλυμμένα με καλυπτρίδα παρατηρήθηκε χρησιμοποιώντας ένα φίλτρο διέγερσης και εκπομπής και ο φωσφορισμός BTPDM1 (Hirakawa et al., 2015) ανιχνεύτηκε χρησιμοποιώντας μικροσκόπιο φθορισμού, BZ-X710 (Keyence Corporation). Οι εικόνες που ελήφθησαν από το ανεστραμμένο μικροσκόπιο φθορισμού ρυθμίστηκαν για φωτεινότητα και αντίθεση χρησιμοποιώντας το λογισμικό ανάλυσης BZ-X.
2.4|Ανοσοκυτταροχημεία
Κύτταρα σε καλυπτρίδα καλλιεργήθηκαν με 200 μΜ HCl πιμονιδαζόλης (HP3-100, Hypoxyprobe, Inc.) σε DMEM/F12 χωρίς ερυθρό φαινόλης για 1 ώρα, μετά την οποία η καλυπτρίδα περιστράφηκε και προσαρτήθηκε σε ένα καλυμμένο γυάλινο δίσκο, όπως που περιγράφηκε προηγουμένως. Τα κύτταρα στη συνέχεια καλλιεργήθηκαν σε DMEM/F12 χωρίς ερυθρό φαινόλης για μια καθορισμένη περίοδο. Όταν δεν χρησιμοποιήθηκε αντιχρώση με πιμονιδαζόλη, η προεπεξεργασία με πιμονιδαζόλη παραλείφθηκε.
Μετά την ολοκλήρωση της περιόδου καλλιέργειας, κάθε καλυπτρίδα συλλέχθηκε και τα κύτταρα στερεώθηκαν αμέσως με μεθανόλη/ακετόνη (1:1) σε πάγο, όπου παρέμειναν για 30 λεπτά. Μετά από δύο φορές πλύσιμο με αλατούχο διάλυμα Dulbecco's ρυθμισμένο με φωσφορικά (PBS) (D5652, Sigma Aldrich), η κυτταρική μεμβράνη διαπερατήθηκε για 30 λεπτά, επωάστηκε με 5 τοις εκατό αλβουμίνη ορού βοοειδών (BSA) (A3059, Sigma Aldrich) για 30 λεπτά κάθε φορά, με μπλοκ πρωτεΐνης χωρίς ορό (X0909, DAKO) για 10 λεπτά. Τα κύτταρα χρωματίστηκαν με ένα πρώτο αντίσωμα και στη συνέχεια με ένα δεύτερο, φθορίζον αντίσωμα. Ο κατάλογος των πρώτων αντισωμάτων δίνεται στον Πίνακα S1. Η πολυκλωνική ανοσοσφαιρίνη κατά του κουνελιού FITC-χοίρου (F0205, αραίωση 1:20, DAKO) χρησιμοποιήθηκε ως το πρώτο αντίσωμα εάν ο ξενιστής ήταν κουνέλι. Το φθορίζον αντίσωμα Alexa Fluor 594 στρεπταβιδίνη (S11227, αραίωση 1:500, Thermo Fisher Scientific) χρησιμοποιήθηκε ως το πρώτο αντίσωμα εάν ο ξενιστής ήταν ποντικός, ακολουθούμενο από βιοτινυλιωμένο αντι-ποντικού IgG (H συν L) (BA{{{23} }, αραίωση 1:1000, Vector Laboratories), ως το δεύτερο αντίσωμα. Πραγματοποιήθηκε πυρηνική χρώση χρησιμοποιώντας τριυδροχλωρικό διςβενζιμίδιο Η 33342 (Β2261, Sigma Aldrich) για κάθε δείγμα.
Τα σήματα φθορισμού παρατηρήθηκαν χρησιμοποιώντας ένα ανεστραμμένο μικροσκόπιο φθορισμού, BZ-X710 (Keyence Corporation) με τα ακόλουθα φίλτρα: Texas Red με μήκος κύματος διέγερσης (Ex) 560/40 nm, μήκος κύματος εκπομπής (Em) 630/75 nm, GFP ( Π.χ.: 470/40 nm, Em: 525/50 nm) και DAPI (Π.χ.: 360/40 nm, Em: 460/50 nm). Οι εικόνες προσαρμόστηκαν για φωτεινότητα και αντίθεση χρησιμοποιώντας το λογισμικό ανάλυσης BZ-X.
2,5|ICC HIF κυττάρων HK-2 που υποβλήθηκαν σε επεξεργασία με χλωριούχο κοβάλτιο
Η εναλλακτική μέθοδος τροποποιήθηκε για να παραχθεί ένα μοντέλο καλυπτρίδας κυττάρων HK-2 που υποβλήθηκαν σε επεξεργασία με χλωριούχο κοβάλτιο. Τα κύτταρα HK-2 σπάρθηκαν σε μισοσυρρέουσα πυκνότητα (2,5 × 105/πιάτο) σε καλυπτρίδα την ημέρα 1 και υποβλήθηκαν σε επεξεργασία με 300 μΜ εξαένυδρο χλωριούχο κοβάλτιο (C 8661, Sigma Aldrich) για 16 ώρες την Ημέρα 2. Την Ημέρα 3, η καλυπτρίδα αντιστράφηκε για να προσκολληθούν οι επιφάνειες των κυψελών στον πυθμένα ενός νέου γυάλινου δίσκου 27 mm για 3 ώρες και πραγματοποιήθηκε το ICC του HIF.
2.6|Western blotting
Για τη διερεύνηση της συσσώρευσης HIF{{0}} υπό διαφορετικές τάσεις οξυγόνου και σε διαφορετικά επίπεδα pH, 1.0 × 106 HK-2 κύτταρα ανά δίσκο καλλιέργειας 10 cm. επωάστηκαν είτε υπό νορμοξία, 2 τοις εκατό οξυγόνο, 1 τοις εκατό οξυγόνο ή ανοξία, για 5 ώρες ή σε DMEM/F12 σε ρΗ 7,4, ρΗ 6,0 ή ρΗ 5,0 για 5 ώρες.
Αυτά τα κύτταρα υποβλήθηκαν σε λύση σε ρυθμιστικό διάλυμα RIPA που περιείχε 50 mM Tris-ρυθμιστικό διάλυμα (ρΗ 8.0), 150 mM NaCl, 0.5 τοις εκατό w/v νατρίου. δεοξυχολικό, 0,1 w/v τοις εκατό SDS και 1,0 w/v τοις εκατό NP40.
Για western blotting, ρυθμιστικό δείγματος SDS που περιέχει {{0}},35 M Tris-HCl (pH 6,8), 10 τοις εκατό SDS, 36 τοις εκατό γλυκερίνη, 0,012 τοις εκατό μπλε βρωμοφαινόλης και 0,1 M διθειοθρεϊτόλη (DTT) προστέθηκε στις πρωτεΐνες. Οι πρωτεΐνες που περιείχαν ρυθμιστικό δείγματος SDS εκλούστηκαν με βρασμό στους 95 βαθμούς για 5 λεπτά.
Οι πρωτεΐνες διαχωρίστηκαν με ηλεκτροφόρηση σε πηκτώματα πολυακρυλαμιδίου 10 τοις εκατό SDS. Οι πρωτεΐνες στη συνέχεια μεταφέρθηκαν σε μεμβράνη AmershamTM HybondTM PVDF (10600023, GE Healthcare) σε ρυθμιστικό μεταφοράς (48 mM ρυθμιστικό διάλυμα Tris-base, 39 mM γλυκίνη, 0,04 τοις εκατό SDS και 20 ν/ν τοις εκατό μεθανόλη) χρησιμοποιώντας ένα Trans-Blot® Σύστημα μεταφοράς TurboTM (Bio-Rad). Οι μεμβράνες επωάστηκαν σε θερμοκρασία δωματίου με πρωτεύοντα αντισώματα, αντίσωμα anti-HIF1 (Σημ.100-134, αραίωση 1:500, Novus Biologicals, RRID: AB_350071) και αντίσωμα κατά της ακτίνης (A2066 , 1:2000 αραίωση, Sigma Aldrich, RRID: AB{_476693), και στη συνέχεια στο δευτερεύον αντίσωμα, πολυκλωνική ανοσοσφαιρίνη κατσίκας κατά κουνελιού/HRP (P0448, αραίωση 1:10000, DAKO, RRID: AB{{26 }}). Για την ανίχνευση χρησιμοποιήθηκε το υπόστρωμα Western Blotting PierceTM ECL Plus (32132, ThermoFisher Scientific). Παρατηρήθηκε χημειοφωταύγεια χρησιμοποιώντας αναλυτή Luminoimage ImageQuantLAS4000mini (GE Healthcare). Η αναπαραγωγιμότητα επιβεβαιώθηκε με την εκτέλεση τουλάχιστον τριών ανεξάρτητων πειραμάτων. Η ένταση των ζωνών ποσοτικοποιήθηκε χρησιμοποιώντας το λογισμικό Εθνικών Ινστιτούτων Υγείας ImageJ (Schneider et al., 2012).
2.7|Δοκιμασία αναφοράς Luciferase
Πραγματοποιήθηκε μια δοκιμασία αναφοράς λουσιφεράσης για τη μέτρηση της συσσώρευσης HIF1 σε επώαση ομογενούς υποξικής καλλιέργειας. Κατασκευάσαμε προηγουμένως ένα επισημασμένο γονίδιο λουσιφεράσης που οδηγείται από ένα στοιχείο που ανταποκρίνεται στην υποξία (HRE) και αναπτύξαμε τον φορέα αναφοράς που ανταποκρίνεται στην υποξία (Δομή διαγονιδίου). Αυτό κατασκευάστηκε από διαδοχικά αντίγραφα του HRE από το γονίδιο του αγγειακού ενδοθηλιακού αυξητικού παράγοντα αρουραίου που υποκλωνοποιήθηκε στην περιοχή 5' της μονάδας μεταγραφής am CMV-προαγωγέα-λουσιφεράσης (pre-Luc) (Chiang et al., 2011, Tanaka et al. al., 2004).
Κύτταρα ΗΚ{{0}} σε συγκέντρωση 1,0 χ 105 ανά φρεάτιο παρασκευάστηκαν σε 12-πλάκες καλλιέργειας φρεατίων (150628, Thermo Fisher Scientific). Τα κύτταρα συνεπιμολύνθηκαν με 500 ng φορέων pGL3-Βασικών φορέων HRE-λουσιφεράσης και 30 ng φορέων ελέγχου λουσιφεράσης pRL-SV40 Renilla (Promega), χρησιμοποιώντας 2 μl αντιδραστηρίου επιμόλυνσης FuGENE® HD (E2311, Promega) ανά Καλά. Ως αρνητικός μάρτυρας χρησιμοποιήθηκαν κύτταρα HK-2 που συνεπιμολύνθηκαν με 500 ng pGL3-Βασικοί φορείς λουσιφεράσης πυγολαμπίδας και 30 ng φορέων ελέγχου pRL-SV40 Renilla λουσιφεράσης (Promega).
Τα διαμολυνθέντα κύτταρα επωάστηκαν υπό νορμοξία, 2 τοις εκατό υποξία, 1 τοις εκατό υποξία, ή σάκο ανοξίας, για 5 ώρες. Τα κύτταρα στη συνέχεια συλλέχθηκαν χρησιμοποιώντας 100 μΙ ρυθμιστικού διαλύματος παθητικής λύσης πρωτεϊνών, για τον προσδιορισμό διπλής λουσιφεράσης. Για τις μετρήσεις χρησιμοποιήθηκε ένα φωτόμετρο LB9507 (EG και Berthold). Για να διορθωθεί η αποτελεσματικότητα της επιμόλυνσης, η σχετική τιμή της μονάδας φωτός της λουσιφεράσης της πυγολαμπίδας διαιρέθηκε με αυτή της λουσιφεράσης Renilla.

cistanche για εκδ
2.8|Ανάλυση απόπτωσης
Τα καλλιεργημένα κύτταρα καλύφθηκαν με καλυπτρίδα για 0 λεπτά, 15 λεπτά, 30 λεπτά, 1 ώρα, 3 ώρες, 6 ώρες και 24 ώρες και στη συνέχεια συλλέχθηκαν χρησιμοποιώντας θρυψίνη. Κύτταρα που υποβλήθηκαν σε επεξεργασία με 3 τοις εκατό υπεροξείδιο του υδρογόνου (081- 04215, Wako Pure Chemical Industries, Ltd.) για 30 λεπτά παρασκευάστηκαν ως αποπτωτικός έλεγχος. Πραγματοποιήθηκε ποσοτική ανάλυση της απόπτωσης χρησιμοποιώντας κιτ Muse Annexin V και Dead Cell (MCH100105, Millipore) σε αναλυτή κυττάρου Muse™ (Milipore), σύμφωνα με τις οδηγίες του κατασκευαστή.
2,9|Ποσοτική PCR σε πραγματικό χρόνο (qRT-PCR)
Η εξαγωγή ολικού RNA και η σύνθεση cDNA πραγματοποιήθηκαν σύμφωνα με τις οδηγίες του κατασκευαστή για το RNAiso Plus (9109, Takara) και το PrimeScript™ RT Master Mix (RR036B, Perfect Real Time) (Takara) αντίστοιχα. Πραγματοποιήθηκε PCR σε πραγματικό χρόνο χρησιμοποιώντας THUNDERBIRD SYBR qPCR Mix (QPS{3}}, Toyobo) στο σύστημα ανίχνευσης PCR πραγματικού χρόνου CFX Connect (Bio-Rad). Τα επίπεδα μεταγραφής κανονικοποιήθηκαν στο επίπεδο έκφρασης mRNA της -ακτίνης. Η qRT-PCR πραγματοποιήθηκε εις τριπλούν χρησιμοποιώντας ειδικούς για γονίδιο εκκινητές. Το HIF-1 ενισχύθηκε χρησιμοποιώντας εκκινητές προς τα εμπρός, 5′-CCATTAGAAAGCAGTTCCGC-3′ και αντίστροφα, 5′-TGGGTAGGAGATGGAGATGC-3′. -ακτίνη ενισχύθηκε χρησιμοποιώντας εκκινητές 5'-TCCCCCAACTTGA GATGTATGAAG-3' και αντίστροφα 5'-AACTGGTCTCAAG TCAGTGTACAGG-3'.
2.10|Επιμόλυνση με siRNA
Για τη διερεύνηση της επαγόμενης από RNAi καταστροφής HIF-1 σε κύτταρα HK-2, παρασκευάστηκαν 5.0 × 104 HK-2 κύτταρα ανά φρεάτιο σε πλάκες έξι φρεατίων. Δύο είδη RNAi—HIF-1 siRNA (siHIF-1 #1 [HSS104774, Thermo Fisher Scientific] και siHIF-1 #2 [HSS104775, ThermoFisher Scientific])—χρησιμοποιήθηκαν με το Lipofectamine RNAiMAX Αντιδραστήριο επιμόλυνσης (Thermo Fisher Scientific). Ως αρνητικός έλεγχος, χρησιμοποιήθηκε Stealth RNAi™ siRNA Negative Control Med GC Duplex #3 (12935-113). 1,5 μl από κάθε siRNA και 5 μl RNAiMAX αναμίχθηκαν. Τα επιμολυσμένα με siRNA κύτταρα επωάστηκαν υπό νορμοξικές ή υποξικές (1 τοις εκατό O2) συνθήκες για 48 ώρες και το RNA εκχυλίστηκε. Η αποτελεσματικότητα του knockdown-HIF-1 εξετάστηκε χρησιμοποιώντας qRT-PCR.
2.11|Ζωντανή απεικόνιση των επιδράσεων μιας βαθμίδας PH
Οραματίσαμε την ενδοκυτταρική κλίση του pH των ζωντανών κυττάρων κάτω από μια καλυπτρίδα. Τα κύτταρα υποβλήθηκαν σε επεξεργασία με pHrodo Green AM Intracellular pH Indicator (p35373, ThermoFisher Scientific) σύμφωνα με τις οδηγίες του κατασκευαστή, πριν από την εφαρμογή του μοντέλου καλυπτρίδας. Ένα ανεστραμμένο μικροσκόπιο φθορισμού, BZ-X710 (Keyence Corporation) με φίλτρο GFP χρησιμοποιήθηκε για την παρατήρηση της χρονικής μετάβασης της βαθμίδας έντασης φθορισμού κάτω από μια καλυπτρίδα.
2.12|Ποσοτική ανάλυση του δακτυλίου HIF
2.12.1|Η τοποθεσία του δαχτυλιδιού HIF
Μετρήσαμε την απόσταση των δακτυλίων HIF και των θετικών στην πιμονιδαζόλη περιοχών από τις άκρες καλυπτρίδας χρησιμοποιώντας το ImageJ, ως εξής. Προσδιορίστηκαν οι περιοχές των εξωτερικών και εσωτερικών κύκλων του δακτυλίου HIF και του θετικού στην πιμονιδαζόλη κύκλου και υπολογίστηκε η ακτίνα κάθε κύκλου. Κάθε τιμή αφαιρέθηκε από τα 7,5 mm, που είναι η ακτίνα μιας καλυπτρίδας 15 mm, για να υπολογιστεί η απόστασή της από ένα άκρο καλυπτρίδας. Πραγματοποιήθηκαν τρία ανεξάρτητα πειράματα ICC του HIF σε κάθε κατάσταση.
2.12.2|Ορισμός του δαχτυλιδιού HIF
Χρησιμοποιήσαμε φθορίζουσες εικόνες που ελήφθησαν από ένα μοντέλο καλυπτρίδας που επωάστηκε υπό νορμοξία και ουδέτερο pH. Ορίσαμε την τοποθεσία του δακτυλίου HIF και το εξωτερικό και το εσωτερικό του ως 2,5–3.{3}} κλίμακα (0.22–0.45 mm), 0.5 –1.{11}} κλίμακα (1,12– 1,35 mm) και 5.{17}}–5,5 κλίμακα (2,24–2,47 mm) από ένα άκρο καλυπτρίδας, αντίστοιχα, χρησιμοποιώντας ImageJ. Μετρήσαμε πέντε τοποθεσίες σημάτων HIF-1 ανά δείγμα και υπολογίσαμε τον μέσο όρο. Πραγματοποιήθηκαν τρία ανεξάρτητα πειράματα ICC του HIF.

εκχύλισμα κιστάνσε σε σκόνη
2.13|Μέτρηση πίεσης οξυγόνου με εικόνα PLIM
2.13.1|Κατασκευή γραμμής βαθμονόμησης για τη μέτρηση της πίεσης οξυγόνου
Δημιουργήθηκε μια καμπύλη βαθμονόμησης κυττάρων HK-2, με βάση τη μέθοδο που περιγράφεται στην προηγούμενη αναφορά μας (Yoshihara et al., 2015). Κύτταρα HK-2 φορτωμένα με 500 nM BTPDM1 για 30 λεπτά καλλιεργήθηκαν σε επωαστήρα πολλαπλών αερίων με δυνατότητα αλλαγής συγκέντρωσης οξυγόνου εξοπλισμένο με ένα ανεστραμμένο μικροσκόπιο φθορισμού που ήταν συνδεδεμένο με το σύστημα μέτρησης διάρκειας ζωής. Μια γραμμή βαθμονόμησης που βασίζεται σε αναλύσεις Stern-Volmer κατασκευάστηκε χρησιμοποιώντας τη διάρκεια ζωής φωσφορισμού (PL) των κυττάρων HK{10}} κάτω από πολλές διαφορετικές τάσεις οξυγόνου χρησιμοποιώντας
Εξίσωση (1)

όπου το τp αντιπροσωπεύει το PL στο pO2, το τ0 αντιπροσωπεύει το PL στην αποοξυγόνωση, το kq αντιπροσωπεύει τη σταθερά του ρυθμού σβέσης και το pO2 αντιπροσωπεύει τη μερική πίεση του οξυγόνου. Χρησιμοποιώντας αυτή τη γραμμή βαθμονόμησης, η πίεση οξυγόνου μπορούσε να υπολογιστεί από το PL.
2.13.2|Εικόνα PLIM μοντέλου καλυπτρίδας
Παρασκευάστηκαν κύτταρα HK-2 φορτωμένα με 500 nM BTPDM1 για 30 λεπτά. Κατασκευάστηκε ένα μοντέλο καλυπτρίδας και καλλιεργήθηκε σε επωαστήρα πολλαπλών αερίων με δυνατότητα αλλαγής της συγκέντρωσης O2 εξοπλισμένο με ανεστραμμένο μικροσκόπιο φθορισμού, συνδεδεμένο με το σύστημα μέτρησης διάρκειας ζωής.
Οι εικόνες με μικροσκόπιο απεικόνισης διάρκειας ζωής φωσφορισμού (PLIM) καταγράφηκαν χρησιμοποιώντας ένα ανεστραμμένο μικροσκόπιο φθορισμού εξοπλισμένο με σύστημα ομοεστιακής σάρωσης (Hirakawa et al., 2018). Οι εικόνες PLIM ελήφθησαν μετά από επώαση 30 λεπτών σε 21 τοις εκατό Ο2 ή 4 τοις εκατό Ο2. Τέσσερις εικόνες PLIM ανά δείγμα, από την άνω, κάτω, αριστερή και δεξιά περιοχή κοντά στην άκρη της καλυπτρίδας, λήφθηκαν, για να προσδιοριστεί η μέση τιμή PL, λαμβάνοντας υπόψη τη διακύμανση των PL σε μια καλυπτρίδα.
2.13.3|Αναγνώριση του δακτυλίου HIF σε μια εικόνα PLIM
Η πιμονιδαζόλη ήταν θετική κάτω από 10 mmHg πίεσης οξυγόνου. Το ισοδύναμο PL των 10 mmHg πίεσης οξυγόνου ήταν 4034,6 ns, σύμφωνα με τη γραμμή βαθμονόμησης, επομένως η εξωτερική γραμμή του κύκλου της πιμονιδαζόλης στην εικόνα PLIM μπορούσε να αναγνωριστεί. Στη συνέχεια, οι θέσεις των εξωτερικών και εσωτερικών δακτυλίων HIF στην εικόνα PLIM μπορούσαν να βρεθούν χρησιμοποιώντας ποσοτική ανάλυση απόστασης. Μετρήσαμε το εύρος των μέσων PLs ισοδύναμων με τον δακτύλιο HIF σε 21 τοις εκατό O2 και 4 τοις εκατό O2.
2.13.4|Μέτρηση της πίεσης οξυγόνου του δακτυλίου HIF
Υπολογίσαμε το εύρος των πιέσεων οξυγόνου του δακτυλίου HIF από τα PLs, χρησιμοποιώντας τη γραμμή βαθμονόμησης. Οι εικόνες PLIM αναλύθηκαν χρησιμοποιώντας το SPCImage 5.0 (Becker & Hickl GmbH).
2.14|Στατιστική ανάλυση
Το τεστ Dunnett χρησιμοποιήθηκε για τη σύγκριση των πειραματικών ομάδων και των ομάδων ελέγχου και οι τιμές < 0,05="" θεωρήθηκαν="" ότι="" υποδεικνύουν="" στατιστικά="" σημαντικές="" διαφορές.="" χρησιμοποιήθηκαν="" τα="" τεστ="" t="" student="" για="" τη="" σύγκριση="" τριών="" ή="" περισσότερων="" ομάδων="" και="" εφαρμόστηκε="" η="" προσαρμοσμένη="" τιμή="" p="" bonferroni.="" όλες="" οι="" στατιστικές="" αναλύσεις="" πραγματοποιήθηκαν="" χρησιμοποιώντας="" jmp="" pro="" ver13.2.1="" (sas).="" οι="" τιμές="" θεωρήθηκε="" ότι="" προέρχονται="" από="" έναν="" κανονικά="" κατανεμημένο="" πληθυσμό="" και="" εμφανίζονται="" ως="" μέση="" ±="" τυπική="" απόκλιση="">

τι είναι ένα cistanche
3|ΑΠΟΤΕΛΕΣΜΑΤΑ
3.1|Σχηματισμός βαθμίδας οξυγόνου στο μοντέλο υποαιμάτωσης
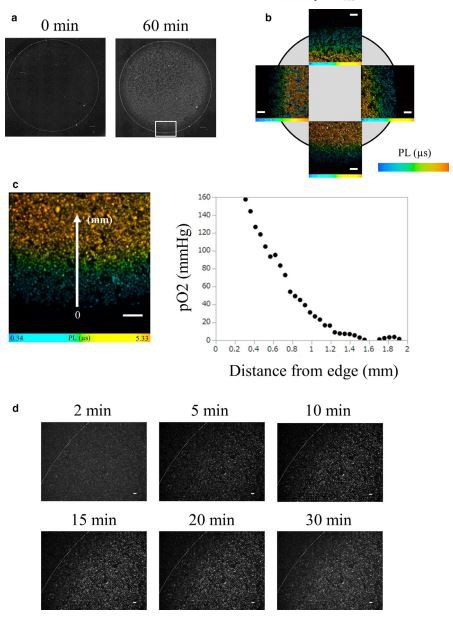
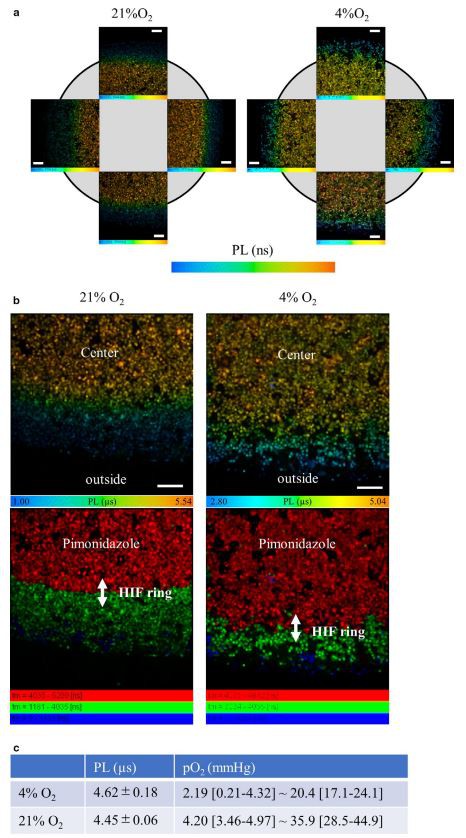
Επιβεβαιώσαμε την ύπαρξη βαθμίδας οξυγόνου στο μοντέλο υποαιμάτωσης που προκαλείται από την τοποθέτηση καλυπτρίδας αξιολογώντας απευθείας την τάση οξυγόνου, χρησιμοποιώντας φωσφορισμό. Η μέτρηση της έντασης του φωσφορισμού μπορεί να προβλέψει μια κατά προσέγγιση τάση στην πίεση του οξυγόνου (Hirakawa et al., 2015; Yoshihara et al., 2015). Παρατηρήσαμε την ένταση φωσφορισμού ενός μοντέλου καλυπτρίδας κυττάρων HK-2 που υποβλήθηκαν σε επεξεργασία με BTPDM1. Οι εικόνες της έντασης του φωσφορισμού έδειξαν υποξία στο μεγαλύτερο μέρος της περιοχής μέσα στην καλυπτρίδα, αλλά όχι υποξία κοντά στην άκρη, μια παρατήρηση που υποδηλώνει την ύπαρξη βαθμίδας οξυγόνου γύρω από την άκρη της καλυπτρίδας σε κύτταρα HK-2 που καλύπτονται με καλυπτρίδα (Εικόνα 1α). Δεδομένου ότι η ένταση του φωσφορισμού εξαρτάται από τη συγκέντρωση του ανιχνευτή και από τον χρόνο διέγερσης, μια μέτρηση διάρκειας ζωής φωσφορισμού (PL) είναι χρήσιμη για την ποσοτική ανάλυση της πίεσης του οξυγόνου (Yoshihara et al., 2015). Έτσι, για την ποσοτική μέτρηση της τάσης οξυγόνου των καλλιεργημένων κυττάρων γύρω από την άκρη μιας καλυπτρίδας, λάβαμε εικόνες PLIM κυττάρων HK-2 καλυμμένων με καλυπτρίδα για 30 λεπτά (Εικόνα 1β). Το PL επεκτάθηκε καθώς η απόσταση από την άκρη της καλυπτρίδας αυξανόταν. Επιβεβαιώσαμε ότι η τάση οξυγόνου, που υπολογίστηκε χρησιμοποιώντας μια γραμμή βαθμονόμησης (Εικόνα S3), μειώθηκε όσο αυξανόταν η απόσταση από την άκρη της καλυπτρίδας, παρέχοντας στοιχεία για την ύπαρξη βαθμίδας οξυγόνου γύρω από την άκρη της καλυπτρίδας (Εικόνα 1γ). Η εξέταση του χρονικού προφίλ της έντασης του φωσφορισμού έδειξε ότι η βαθμίδα οξυγόνου άρχισε να σχηματίζεται 10 λεπτά μετά την τοποθέτηση καλυπτρίδας
(Εικόνα 1δ).
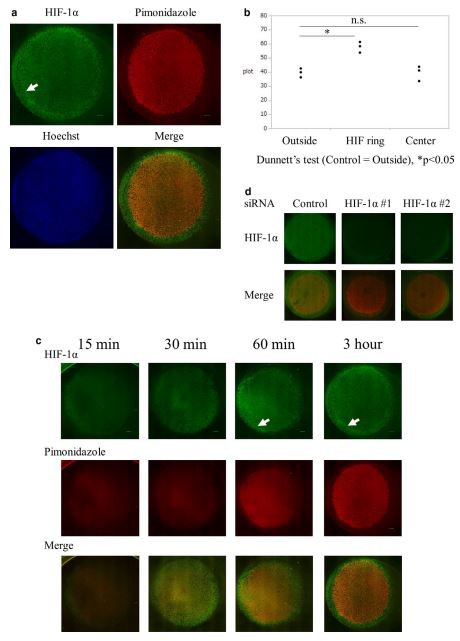
3.2|Μοναδική κατανομή HIF-1 στο μοντέλο hypoperfusion "HIF ring"
Εξετάσαμε την κατανομή HIF-1 στο μοντέλο υποαιμάτωσης με βαθμίδα οξυγόνου. Το ICC του HIF-1 στα κύτταρα HK-2 έδειξε μια ενίσχυση σε σχήμα ντόνατς στην άκρη της θετικής στην πιμονιδαζόλη περιοχής, την οποία ονομάσαμε "δακτύλιος HIF" (Εικόνα 2α). Η ένταση του σήματος HIF-1 ήταν σημαντικά υψηλότερη στον δακτύλιο HIF από ότι στις εσωτερικές ή εξωτερικές περιοχές του (Εικόνα 2β). Αυτό το φαινόμενο επιβεβαιώθηκε χρησιμοποιώντας ICC με άλλο αντίσωμα HIF-1 (Εικόνα S4a) ή άλλες σωληναριακές κυτταρικές σειρές (Εικόνα S4b,c). Πραγματοποιήσαμε επίσης ανάλυση ICC του HIF-1 σε άλλα είδη καλλιεργημένων κυττάρων, όπως τα καρκινικά κύτταρα του τραχήλου της μήτρας HeLa. Αν και η ασθενής προσκόλληση αυτών των κυττάρων σε μια καλυπτρίδα έκανε δύσκολη τη λεπτομερή αξιολόγηση της κατανομής του HIF-1, παρατηρήσαμε μια ενίσχυση σε σχήμα ντόνατς του HIF-1 σε κύτταρα HeLa (Εικόνα S4d).
Ο δακτύλιος HIF και η θετική στην πιμονιδαζόλη περιοχή άρχισαν να σχηματίζονται αρκετές ώρες μετά την τοποθέτηση καλυπτρίδας και ο δακτύλιος HIF εμφανίστηκε στατικός σε 3 ώρες (Εικόνα 2γ). Το knockdown HIF-1 είχε ως αποτέλεσμα την εξαφάνιση του σήματος HIF-1 , συμπεριλαμβανομένου του δακτυλίου HIF (Εικόνα 2δ, Εικόνα S4e), υποδεικνύοντας ότι ο δακτύλιος HIF εξαρτιόταν από το HIF-1 .
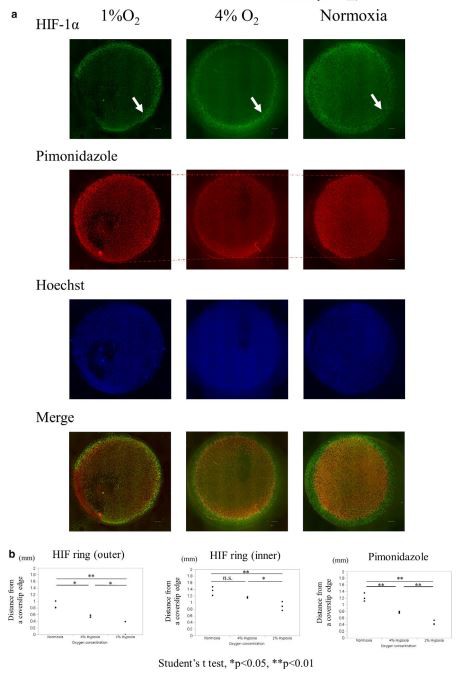
Για να διερευνήσουμε την πιθανότητα ο σχηματισμός δακτυλίου HIF να εξαρτάται από το οξυγόνο, διερευνήσαμε την κατανομή του HIF-1 στο μοντέλο καλυπτρίδας υπό επώαση με διαφορετικές τάσεις οξυγόνου. Τοποθετήσαμε ένα πιάτο σε υποξικούς θαλάμους με διαφορετικές τάσεις οξυγόνου αμέσως μετά την κατασκευή ενός μοντέλου καλυπτρίδας. Κατά τη διάρκεια της υποξικής επώασης, παρατηρήσαμε ότι τόσο ο δακτύλιος HIF όσο και η θετική στην πιμονιδαζόλη περιοχή φάνηκαν να επεκτείνονται προς τα έξω (Εικόνα 3α). Μετρήσαμε την απόσταση κάθε δακτυλίου HIF και περιοχής θετικής για πιμονιδαζόλη από ένα άκρο καλυπτρίδας υπό νορμοξία, 4 τοις εκατό O2 και 1 τοις εκατό O2 επώαση. Τόσο ο δακτύλιος HIF όσο και η θετική στην πιμονιδαζόλη περιοχή επεκτάθηκαν προς τα έξω καθώς μειώθηκε η περιβάλλουσα τάση οξυγόνου (Εικόνα 3β). Αυτά τα αποτελέσματα έδειξαν ότι ο δακτύλιος HIF εξαρτιόταν από το HIF-1 και την τάση οξυγόνου.
Για να επιβεβαιώσουμε ότι η συσσώρευση σε σχήμα ντόνατ είναι ένα συγκεκριμένο φαινόμενο του HIF, πραγματοποιήσαμε ICC με γονίδια housekeeping στο μοντέλο καλυπτρίδας. Τα σήματα GAPDH και ακτίνης διατηρήθηκαν σε ολόκληρη την περιοχή μιας καλυπτρίδας και ήταν συγκρίσιμα μεταξύ της περιοχής του δακτυλίου HIF και των άλλων περιοχών (Εικόνα S5a,b).
3.3|Μέτρηση του εύρους πίεσης οξυγόνου του δακτυλίου HIF
Επιβεβαιώσαμε την ενίσχυση σε σχήμα δακτυλίου της συσσώρευσης HIF-1 σε καλλιεργημένα κύτταρα που καλύπτονται με καλυπτρίδα, ένα φαινόμενο που εξαρτάται από την τάση οξυγόνου. Για να προσδιορίσουμε το εύρος της εμπλεκόμενης τάσης οξυγόνου, αναλύσαμε την πίεση οξυγόνου του δακτυλίου HIF χρησιμοποιώντας μια τεχνική διάρκειας ζωής φωσφορισμού. Λάβαμε εικόνες PLIM του μοντέλου καλυπτρίδας μετά από 3{32}} λεπτά επώασης σε 21 τοις εκατό O2 ή 4 τοις εκατό O2 (Εικόνα 4α). Ο δακτύλιος HIF σχηματίστηκε στην άκρη του κύκλου της πιμονιδαζόλης στο ICC του HIF (Εικόνα 3β). Προσδιορίσαμε τη θέση στην εικόνα PLIM που ήταν ισοδύναμη με τη θετική στην πιμονιδαζόλη περιοχή στο ICC του HIF και στη συνέχεια εντοπίσαμε τη θέση που αντιστοιχεί στον δακτύλιο HIF (Εικόνα 4β), χρησιμοποιώντας ποσοτική ανάλυση των δεδομένων απόστασης από τον δακτύλιο HIF και το περιοχή θετική για πιμονιδαζόλη (Εικόνα 3β). Μετρήσαμε επίσης το εύρος των PL του δακτυλίου HIF και στη συνέχεια χρησιμοποιήσαμε μια γραμμή βαθμονόμησης (Εικόνα S3) για να υπολογίσουμε την πίεση οξυγόνου του δακτυλίου HIF σε 21 τοις εκατό O2 (4,20 [3,46–4,97] ~35,9 [28,5–44,9] mmHg) , και 4 τοις εκατό O2 (2,19 [0,21-4,32] ~ 20,4 [17,1-24,1] mmHg) (Εικόνα 4γ).
3.4|Συσσώρευση HIF-1 υπό ομοιογενή τάση οξυγόνου
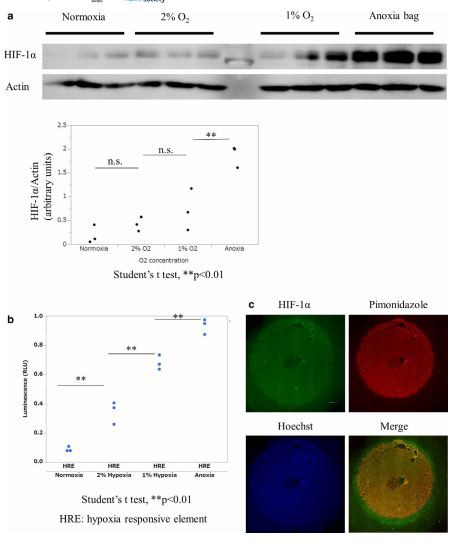
Ενώ τα αδύναμα σήματα του HIF-1 εκτός του δακτυλίου HIF σε ένα μοντέλο καλυπτρίδας μπορούν να αποδοθούν σε ανεπαρκή υποξία, αυτά εντός του δακτυλίου, όπου το HIF-1 θα έπρεπε να είχε ενεργοποιηθεί πιο έντονα από τη χαμηλότερη τάση οξυγόνου, πρέπει να ελέγχεται από ένα ανεξάρτητο από το οξυγόνο φαινόμενο. Για να εξετάσουμε τα φαινόμενα που προκαλούν έλλειψη μέγιστης συσσώρευσης HIF-1 στην ανοξική περιοχή που εμφανίζεται μόνο στο μοντέλο υποαιμάτωσης, εξετάσαμε εάν υπήρχε αντίστροφη σχέση μεταξύ της τάσης οξυγόνου και της συσσώρευσης HIF-1 υπό επώαση με ομοιογενή τάση οξυγόνου. Η ανάλυση κηλίδας Western των προϊόντων λύσης κυττάρων υπό διαφορετικές ομοιογενείς τάσεις οξυγόνου έδειξε αύξηση στη συσσώρευση HIF-1 κατά τη διάρκεια της ανοξικής επώασης (Εικόνα 5α). Η ανάλυση αναφοράς HRE-λουσιφεράσης έδειξε επίσης ότι η συσσώρευση HIF-1 αυξήθηκε με χαμηλότερη τάση οξυγόνου υπό συνθήκες ομοιογενούς τάσης οξυγόνου (Εικόνα 5β). Αυτά τα αποτελέσματα έδειξαν ότι η συσσώρευση HIF-1 εξαρτιόταν από την τάση του οξυγόνου, με τη μέγιστη συσσώρευση να παρατηρείται στο εύρος ανοξικών. Τα χαρακτηριστικά του HIF-1 θα πρέπει να διαφέρουν μεταξύ ενός μοντέλου υποαιμάτωσης και ενός μοντέλου με ομοιογενή τάση οξυγόνου. Υποθέσαμε ότι το μοναδικό φαινόμενο της συσσώρευσης HIF-1 σε αυτό το μοντέλο υποαιμάτωσης μπορεί να προσδιορίζεται από έναν παράγοντα διαφορετικό από την τάση οξυγόνου.
3,5|Ο σχηματισμός δακτυλίου HIF ήταν ανεξάρτητος από το PhD
Εξετάσαμε εάν η υποβάθμιση του HIF-1, ένας πιθανός μηχανισμός σχηματισμού δακτυλίου HIF, ρυθμίστηκε προς τα πάνω εντός του δακτυλίου HIF. Αυτή η ιδέα φαινόταν άκυρη, επειδή η υδροξυλίωση με Ph.D., μια διαδικασία που περιορίζει το ρυθμό της αποδόμησης του HIF, απαιτεί οξυγόνο ως υπόστρωμα. Το χλωριούχο κοβάλτιο χρησιμοποιείται ευρέως ως χημικός σταθεροποιητής HIF. Κατασκευάσαμε ένα μοντέλο καλυπτρίδας κυττάρων HK-2 που υποβλήθηκαν σε επεξεργασία με χλωριούχο κοβάλτιο και πραγματοποιήσαμε ανάλυση ICC του HIF. Το σήμα HIF-1 δεν αυξήθηκε μέσα στον δακτύλιο HIF, κάτι που έγινε ασαφές λόγω του αυξημένου σήματος του HIF-1 έξω από τον δακτύλιο (Εικόνα 6γ). Το ICC των HK-2 κυττάρων με εξουδετέρωση της PHD2, η οποία πιστεύεται ότι είναι η πρωτογενής HIF προλυλ υδροξυλάση σε πειράματα κυτταροκαλλιέργειας (Strowitzki et al., 2019), παρήγαγε παρόμοια αποτελέσματα (Εικόνα S6). Αυτά τα αποτελέσματα έδειξαν ότι ο άξονας PHD-VHL της αποικοδόμησης του HIF δεν είχε σχέση με το σχηματισμό δακτυλίου HIF.
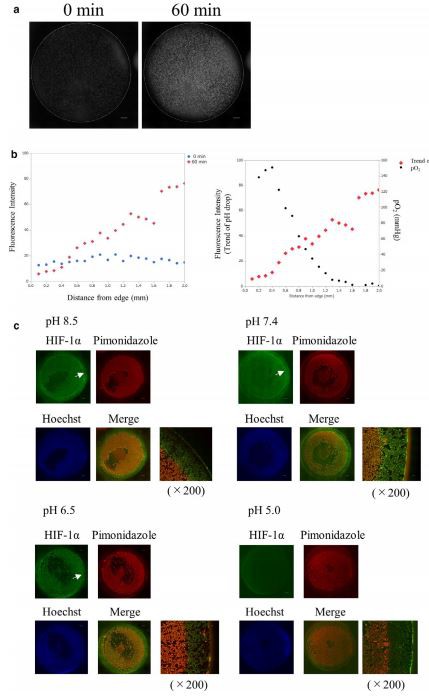
3.6|Επίδραση του pH στη συσσώρευση HIF-1
Μια προηγούμενη αναφορά περιέγραφε τη χρήση ενός μοντέλου καλυπτρίδας καρδιακών μυοκυττάρων που παρουσίαζαν πτώση του pH μέσα στην καλυπτρίδα (Pitts & Toombs, 2004). Ερευνήσαμε το pH κάτω από μια καλυπτρίδα και την επίδρασή του στον σχηματισμό δακτυλίου HIF. Αντιμετωπίσαμε κύτταρα HK-2 με έναν ενδοκυτταρικό δείκτη pH, η ένταση φθορισμού του οποίου επιτρέπει την αξιολόγηση του pH στα κύτταρα. Η ζωντανή απεικόνιση έδειξε ότι το pH μειώθηκε στο μεγαλύτερο μέρος της εσωτερικής περιοχής, αλλά όχι κοντά στην άκρη της καλυπτρίδας, υποδηλώνοντας την ύπαρξη κλίσης pH γύρω από την άκρη στο μοντέλο καλυπτρίδας (Εικόνα 6α). Η ποσοτική ανάλυση της συσχέτισης μεταξύ της έντασης φθορισμού και της απόστασης από ένα άκρο καλυπτρίδας έδειξε ότι η πρώτη ήταν ανυψωμένη καθώς η απόσταση αυξανόταν, μια παρατήρηση που υποστήριξε την ύπαρξη βαθμίδων pH και οξυγόνου γύρω από την άκρη της καλυπτρίδας (Εικόνα 6β). Η ανάλυση Western blot των κυτταρολυμάτων υπό ομοιογενείς συγκεντρώσεις οξυγόνου βρήκε ότι η επώαση με μέσο pH 5,0 κατέστειλε τη συσσώρευση HIF-1 υπό συνθήκες υποξίας (Εικόνα S7a–d). Επιβεβαιώσαμε επίσης ότι η συσσώρευση HIF-1 υπό υποξία υπό διαφορετικές συνθήκες pH μειώθηκε κάτω από το pH 6,0 (Εικόνα S8a–c).
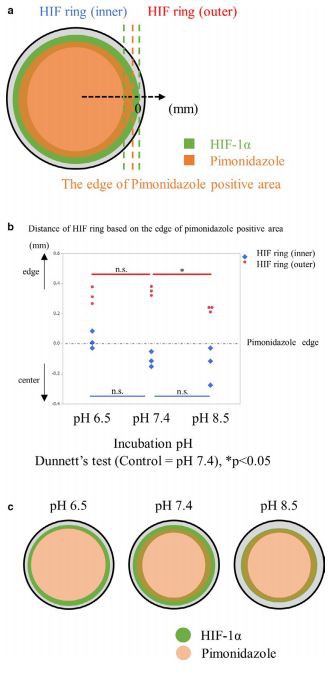
Μια αναφορά τόνισε τη σημασία των ήπιων όξινων συνθηκών, σε pH περίπου 6.0. Σύμφωνα με αυτή τη μελέτη, η επαναοξυγόνωση μετά την υποξία οξίνισε τα μέσα, γεγονός που προκάλεσε πυρηνική δέσμευση του VHL. Με τη σειρά του, η αποικοδόμηση του HIF αποτράπηκε σε μυοσωληνάρια C2C12, νευρώνες PC12 και 786-0 καρκινικά κύτταρα νεφρού (Mekhail et al., 2004). Στη μελέτη μας, δεν υπήρξε αλλαγή στην κατανομή VHL στα σωληναριακά κύτταρα μεταξύ των περιοχών με συσσώρευση HIF-1 και εκείνων στις οποίες καταστέλλεται, σε ένα μοντέλο καλυπτρίδας με τιμές pH από 5.{31}} έως 7,4. (Εικόνα S9a–c). Τα σωληνοειδή κύτταρα εκτίθενται σε ένα ευρύ φάσμα συνθηκών pH (Burke et al., 1999; Pavuluri et al., 2019; Raghunand et al., 2003), έτσι ερευνήσαμε τη διακύμανση του δακτυλίου HIF σε μέσα διαφορετικού pH τιμές μεταξύ 5,0 και 8,5. Ο δακτύλιος HIF παρατηρήθηκε καθαρά σε μέσα με ρΗ 8,5 και 7,4 (Εικόνα 6γ). Ο δακτύλιος HIF υπήρχε επίσης σε pH 6,5 αλλά επισκιάστηκε (Εικόνα 6γ). Το σήμα HIF-1 εξασθενήθηκε σε ολόκληρη την περιοχή μιας καλυπτρίδας σε pH 5,0. (Εικόνα 6γ). Πραγματοποιήσαμε περαιτέρω ποσοτική ανάλυση της σχέσης θέσης μεταξύ του δακτυλίου HIF και της άκρης της θετικής στην πιμονιδαζόλη περιοχής (Εικόνα 7α) και ανακαλύψαμε ότι η θέση του δακτυλίου διέφερε ανάλογα με το pH. Ο εσωτερικός κύκλος έτεινε να διαστέλλεται προς τα έξω σε pH 6,5, σε σύγκριση με pH 7,4, ενώ ο εξωτερικός κύκλος συρρικνώθηκε σημαντικά προς τα μέσα σε pH 8,5, με βάση το άκρο της θετικής στην πιμονιδαζόλη περιοχής (Εικόνα 7b,c). Επιβεβαιώσαμε επίσης ότι οι δραστηριότητες των γονιδίων οικιακής φροντίδας διατηρήθηκαν σε ένα μοντέλο καλυπτρίδας υπό όξινη επώαση (Εικόνα S10). Επομένως, το pH φαίνεται να παίζει σημαντικό ρόλο στον μηχανισμό που κρύβεται πίσω από το σχηματισμό του δακτυλίου HIF.
4|ΣΥΖΗΤΗΣΗ
Σε αυτήν τη μελέτη, εντοπίσαμε μια μοναδική κατανομή HIF-1 σε νεφρικά σωληναριακά κύτταρα, χρησιμοποιώντας ένα μοντέλο υποαιμάτωσης που προκαλείται από την τοποθέτηση καλυπτρίδας. Βρήκαμε ότι ο σχηματισμός και η συντήρηση του δακτυλίου HIF ρυθμίζονταν από την πίεση οξυγόνου και το pH, τα οποία υπήρχαν και τα δύο σε μια κλίση στην άκρη της καλυπτρίδας ενός μοντέλου καλυπτρίδας. Με βάση αυτά τα αποτελέσματα, προτείνουμε έναν πιθανό μηχανισμό για το σχηματισμό δακτυλίου HIF, που περιλαμβάνει τη συσσώρευση HIF-1 με μείωση της τάσης οξυγόνου και τη συσσώρευση που καταστέλλεται λόγω χαμηλού pH σε μια ορισμένη απόσταση από μια άκρη καλυπτρίδας (Εικόνα 8 ).
Η υποέγχυση προκαλείται από την αραίωση των μικροαγγείων στη ΧΝΝ (Mimura & Nangaku, 2{{20}}10; Nangaku, 2006). Στην προηγούμενη εργασία μας, χρησιμοποιήσαμε in vivo απεικόνιση για να δείξουμε την παρουσία βαθμίδας οξυγόνου σε νεφρικά σωληναριακά κύτταρα φυσιολογικών νεφρών ποντικού (Hirakawa et al., 2018). Η τάση οξυγόνου αναμένεται επίσης να είναι ετερογενής στα σωληναριακά κύτταρα στη ΧΝΝ. Ωστόσο, παραμένει ασαφές εάν η ύπαρξη υποαιμάτωσης με βαθμίδα οξυγόνου επηρεάζει το αμυντικό σύστημα έναντι της υποξίας, HIF. Σε αυτή τη μελέτη, διερευνήσαμε την κατανομή του HIF σε καλλιεργημένα κύτταρα εγγύς σωληνάριο υπό ένα μοντέλο υποαιμάτωσης και ανακαλύψαμε ότι η βαθμίδα οξυγόνου σε καλλιεργημένα νεφρικά σωληναριακά κύτταρα μοντελοποιήθηκε με επιτυχία χρησιμοποιώντας μια στρογγυλή γυάλινη καλυπτρίδα. Στοιχεία από πειράματα που χρησιμοποιούν ομογενή τάση οξυγόνου έδειξαν ότι το HIF-1, του οποίου η υδροξυλίωση και η επακόλουθη αποικοδόμηση είναι κυρίως εξαρτώμενες από το οξυγόνο, συσσωρεύτηκε. Αυτή είναι η ποσότητα του HIF-1 που αυξάνεται καθώς μειώνεται η τάση οξυγόνου. Στο μοντέλο μας καλυπτρίδας, ωστόσο, το HIF-1 καταπιεστεί στην ανοξική περιοχή και είχε τη μεγαλύτερη συσσώρευση σε μια ορισμένη απόσταση από μια άκρη καλυπτρίδας. Αυτή η συσσώρευση HIF σε σχήμα ντόνατ δεν έχει παρουσιαστεί ποτέ στο παρελθόν. Δείξαμε ότι η κίνηση του δακτυλίου HIF μπορούσε να παρατηρηθεί ανεξάρτητα από την τάση οξυγόνου της ατμόσφαιρας επώασης, αλλά η θέση του εξαρτιόταν από την τάση οξυγόνου. Το εύρος της τάσης οξυγόνου στον δακτύλιο HIF μετρήθηκε σε περίπου 4–20 mmHg χρησιμοποιώντας PLIM με BTPDM1. Οι περισσότερες προηγούμενες μελέτες, οι οποίες επικεντρώθηκαν σε καλλιεργημένα κύτταρα σε ατμόσφαιρα με ομοιογενή τάση οξυγόνου, διαπίστωσαν ότι η ποσότητα της πρωτεΐνης HIF{12}} αυξήθηκε στις περιοχές υποξίας ή ανοξικής (Ameri et al., 2002· Carrera et al. , 2014). Έτσι, στο μοντέλο μας, ο σχηματισμός δακτυλίου HIF πρέπει να έχει επηρεαστεί από έναν παράγοντα διαφορετικό από την τάση του οξυγόνου. ήταν ανεξάρτητο από το Ph.D., μια διαδικασία που περιορίζει το ρυθμό υποβάθμισης του HIF. Μια σημαντική ανακάλυψη στη διευκρίνιση του μηχανισμού σχηματισμού δακτυλίου HIF ήταν η ανακάλυψη του ρόλου της βαθμίδας pH, καθώς και της βαθμίδας οξυγόνου, στο μοντέλο καλύμματος-χειλών, που περιόρισε την εισροή των μέσων παρόμοια με μια in vivo υποδιάχυση μοντέλο. Σε αυτό το μοντέλο υποαιμάτωσης, το ενδοκυττάριο pH μειώθηκε καθώς η απόσταση από το άκρο καλυπτικής ολίσθησης αυξήθηκε και παρατηρήθηκε μια κλίση pH γύρω από την άκρη της καλυπτρίδας. Δείξαμε ότι η συσσώρευση HIF{18}} καταστέλλεται σε χαμηλό pH, περίπου pH 5,0, σε σύγκριση με την επώαση σε περίπου ουδέτερο pH υπό ομοιογενή τάση οξυγόνου. Το εξωτερικό άκρο του δακτυλίου HIF επεκτάθηκε προς τα έξω σε pH 6,5 και το εσωτερικό άκρο του δακτυλίου HIF συρρικνώθηκε προς τα μέσα σε pH 8,5, με βάση το άκρο της θετικής στην πιμονιδαζόλη περιοχής. Ο δακτύλιος HIF επισκιάστηκε υπό όξινες συνθήκες και το σήμα HIF-1 εξαφανίστηκε σε pH 5,0. Έτσι, διευκρινίσαμε τη σημασία του pH για το σχηματισμό δακτυλίου HIF σε ένα μοντέλο καλυπτρίδας. Δείξαμε την πιθανότητα ότι ο δακτύλιος HIF σχηματίστηκε από την καταστολή της συσσώρευσης HIF-1 από χαμηλό pH μέσα στον δακτύλιο.
Αρκετές προηγούμενες μελέτες με τη μέθοδο της καλυπτρίδας έχουν χρησιμοποιήσει καρκινικά κύτταρα. Σύμφωνα με μια αναφορά που χρησιμοποιεί την κυτταρική σειρά ανθρώπινου ηπατώματος Hep3B, η οποία εκφράζει την οξυγονοεξαρτώμενη μετατόπιση προς το κόκκινο της πράσινης φθορίζουσας πρωτεΐνης (AcGFP1), η ζωντανή απεικόνιση κυττάρων που καλύπτονται με μια ορθογώνια καλυπτρίδα έδειξε μια ερυθρή μετατόπιση καθώς η απόσταση από μια άκρη καλυπτρίδας αυξήθηκε (Takahashi & Sato, 2010). Το φάσμα εκπομπής των κυττάρων του ηπατώματος μετατοπίστηκε από το μήκος κύματος του φθορισμού της πράσινης φθορίζουσας πρωτεΐνης (GFP) σε αυτό του κόκκινου καθώς μειώθηκε η τάση οξυγόνου. Σε μια άλλη μελέτη, η τάση οξυγόνου των κυττάρων SCC-7 με μια στρογγυλή καλυπτρίδα 15-mm μετρήθηκε χρησιμοποιώντας μια τεχνική διάρκειας ζωής φωσφορισμού. Η τάση οξυγόνου ήταν 6,9 mmHg και 166 mmHg, υπολογιζόμενη από την PL, η οποία ήταν 3,89 µs και 893 µs, 0-2 mm εντός και 0-1 mm έξω από την άκρη της καλυπτρίδας, αντίστοιχα (Yoshihara et al., 2015). Η μέθοδος καλυπτρίδας έχει χρησιμοποιηθεί επίσης με καρδιακά μυοκύτταρα, ένα σύστημα που έχει προσελκύσει την προσοχή ως ένα πολλά υποσχόμενο in vivo μοντέλο ισχαιμίας-επαναιμάτωσης. Οι Kelly et al έδειξαν ότι τα μυοκύτταρα που καλύπτονταν με καλυπτρίδα υπέστησαν σημαντικές μορφολογικές αλλαγές με την πάροδο του χρόνου, συνοδευόμενες από αλλαγές στο δυναμικό της μιτοχονδριακής μεμβράνης και στη δυναμική της πλασματικής μεμβράνης, με αποτέλεσμα τελικά τον θάνατο των μυοκυττάρων. Έδειξαν επίσης ότι το ενδοκυτταρικό pH των μυοκυττάρων που καλύπτονται με καλυπτρίδα πέφτει γρήγορα σε περίπου pH 4 στο κέντρο μιας καλυπτρίδας (Pitts & Toombs, 2004). Ένα μοντέλο καλυπτικής ολίσθησης, που αναστέλλει τη διάχυση οξυγόνου ή θρεπτικών ουσιών σε καλλιεργημένα κύτταρα κάτω από μια καλυπτρίδα, μπορεί να μιμηθεί ένα in vivo μοντέλο ισχαιμικών, φυσιολογικών και οριακών ζωνών στο κέντρο, έξω και στην άκρη μιας καλυπτρίδας αντίστοιχα. Αρκετές μελέτες έχουν χρησιμοποιήσει αυτό το μοντέλο ως μοντέλο ισχαιμίας-επαναιμάτωσης μυοκυττάρων in vitro (Chun et al., 2015; Pitts et al., 2008; Solhjoo & O'Rourke, 2015; Wang et al., 2012). Από όσο γνωρίζουμε, η μελέτη μας είναι η πρώτη που εφαρμόζει μια μέθοδο καλυπτρίδας σε σωληνοειδή κύτταρα. Στο σύστημά μας, η απόσταση από ένα άκρο καλυπτρίδας σε μια περιοχή ισοδύναμη με 10 mmHg τάσης οξυγόνου, όπου η πιμονιδαζόλη θα έπρεπε να γίνει θετική, ήταν 1,22 mm και η τάση οξυγόνου μειώθηκε στο μηδέν σε απόσταση 2 mm από την άκρη της καλυπτρίδας . Αυτό το αποτέλεσμα μπορεί να είναι συμβατό με προηγούμενες αναφορές που χρησιμοποιούν καλυπτρίδα περίπου 15 mm, αποδεικνύοντας την ύπαρξη βαθμίδας οξυγόνου τουλάχιστον εντός 2 mm από την άκρη (Akiyama et al., 2018; Yoshihara et al., 2015). Εξετάσαμε τον ρυθμό απόπτωσης των κυττάρων κάτω από καλυπτρίδες (Εικόνα S11) και ανακαλύψαμε ότι η GAPDH και η ακτίνη διατηρήθηκαν ακόμη και μέσα στον δακτύλιο HIF, υποδεικνύοντας ότι ο δακτύλιος HIF δεν προκλήθηκε μόνο από κυτταρική απόπτωση ή θάνατο εντός του δακτυλίου HIF.
Αρκετές μελέτες έχουν μετρήσει την τάση οξυγόνου στα νεφρά χρησιμοποιώντας διαφορετικές μεθόδους. Μερικά παραδείγματα της μέτρησης της τάσης οξυγόνου των φυσιολογικών νεφρών ήταν τα εξής: 50 mmHg και 30 mmHg στον φλοιό και το μυελό χρησιμοποιώντας μικροηλεκτρόδια. και 49 mmHg και 41 mmHg στα τμήματα S1 και S2 των σωληνοειδών κυττάρων του φλοιού χρησιμοποιώντας PLIM (Hirakawa et al., 2017, 2018; Zhang et al., 2014). Η τάση οξυγόνου των άρρωστων νεφρών θα ήταν χαμηλότερη. Σύμφωνα με μια προηγούμενη αναφορά που χρησιμοποιούσε μικροηλεκτρόδια οξυγόνου, οι διαβητικοί αρουραίοι είχαν χαμηλότερη τάση οξυγόνου του νεφρικού παρεγχύματος: 36 mmHg και 11 mmHg στον φλοιό και το μυελό αντίστοιχα (Heyman et al., 2013; Palm et al., 2003). Δεδομένου ότι τα μικροηλεκτρόδια οξυγόνου μετρούν τη μέση τάση του παρεγχυματικού οξυγόνου, αναμένεται μεγαλύτερο εύρος στους άρρωστους νεφρούς. Η ενδοκυτταρική τάση οξυγόνου μειώθηκε στο μηδέν mmHg σε ένα μοντέλο ισχαιμικού νεφρού του οποίου η πλευρική νεφρική αρτηρία και η φλέβα ήταν συσφιγμένες (Hirakawa et al., 2015). Λαμβάνοντας υπόψη αυτά τα ευρήματα, το εύρος της τάσης οξυγόνου στον δακτύλιο HIF, περίπου 4-20 mmHg, φαινόταν να είναι εύλογο in vivo.
Ανακαλύψαμε περαιτέρω ότι το pH επηρέασε τον σχηματισμό δακτυλίου HIF καθώς και την τάση του οξυγόνου. Δεδομένου ότι τα σωληναριακά επιθηλιακά κύτταρα του νεφρού εκτίθενται συνεχώς στο ουροποιητικό υγρό, το pH των σωληναριακών κυττάρων θα πρέπει να επηρεάζεται από αυτό των ούρων. Λαμβάνοντας υπόψη το ευρύ φάσμα του pH στα ούρα, αποφασίσαμε να μελετήσουμε κύτταρα που επωάστηκαν σε ένα εύρος pH 5.0–8,5. Έχουν γίνει μελέτες για το εύρος του pH σε φυσιολογικούς νεφρούς. Μια μελέτη διαπίστωσε ότι το pH του φλοιού ήταν 7,39 ± 0.{{10}}8 και αυτό του μυελού ήταν 7,20 ± {{2{{39} }}}.09, όπως μετρήθηκε χρησιμοποιώντας μικροηλεκτρόδια (Burke et al., 1999). Μια άλλη μελέτη, χρησιμοποιώντας απεικόνιση pH με βάση τη μαγνητική τομογραφία, έδειξε τιμές pH 7,3 ± 0,13 και 7.0 ± 0,29 αντίστοιχα (Raghunand et al., 2003). Αναφέρθηκε ότι το νεφρικό pH μειώθηκε από 6,5 σε 6,32 και σε 5,83 σε σοβαρή περίπτωση, σε μοντέλο ποντικού με ΧΝΝ με οξέωση (Pavuluri et al., 2019). Αυτές οι παρατηρήσεις έδωσαν στοιχεία πτώσης του pH και διακύμανσης στη ΧΝΝ. Ωστόσο, η επίδραση του pH στο HIF-1 που προκαλείται από τη χρόνια υποξία στη ΧΝΝ δεν έχει εξεταστεί επαρκώς. Στην παρούσα μελέτη, παρατηρήθηκε μετατόπιση του δακτυλίου HIF μεταξύ pH 6,5 και pH 7,4, ένα εύρος pH που είναι εύλογο στη ΧΝΝ. Αυτό το αποτέλεσμα υποστήριξε την υπόθεση ότι μια ήπια μείωση του pH επηρεάζει τη συσσώρευση HIF-1 στη ΧΝΝ. Με βάση τις ενδείξεις πτώσης του pH κάτω από 6,0 σε σοβαρές περιπτώσεις ΧΝΝ, είναι επίσης απαραίτητο να αξιολογηθεί η φυσιολογική κατάσταση του HIF{40}} σε χαμηλότερο pH. Αν και έχουν υπάρξει αναφορές ότι ένα όξινο περιβάλλον, ακόμη και σε νορμοξία, σταθεροποιεί το HIF-1, οι περισσότερες από αυτές τις αναφορές διερεύνησαν συνθήκες ήπιας οξύτητας, πάνω από pH 6,0 (Filatova et al., 2016; Mekhail et al., 2004) . Σε αυτήν την εργασία, δείξαμε καταστολή της συσσώρευσης HIF-1 σε σωληνοειδή κύτταρα σε pH 5,0 και εξασθένηση των σημάτων HIF-1 σε ένα μοντέλο καλυπτρίδας που επωάστηκε σε pH 5,0. Επομένως, η μείωση του νεφρικού pH στη ΧΝΝ in vivo μπορεί να συσχετιστεί με ανεπαρκή ενεργοποίηση του HIF, καθώς και με ουραιμικές τοξίνες στον υποξικό νεφρό, επιδεινώνοντας την εξέλιξη της ΧΝΝ (Tanaka et al., 2013).

Η μελέτη μας έχει αρκετούς περιορισμούς. Πρώτον, στην περιοχή της υποαιμάτωσης, τα μέσα καλλιέργειας θα πρέπει να είναι ελλιπή σε θρεπτικά συστατικά, επιπλέον της παρουσίας ανεπάρκειας οξυγόνου και μειωμένου pH. Ωστόσο, είναι δύσκολο να οριοθετηθούν οι επιδράσεις του pH, της τάσης οξυγόνου και άλλων παραγόντων που προκαλούνται από την υποαιμάτωση. Στο σώμα εμφανίζεται ισχαιμία, παθολογική υποαιμάτωση του αίματος που προκαλείται από συνδυασμό χαμηλού οξυγόνου και χαμηλών θρεπτικών συστατικών, σε όργανα και κύτταρα. Είναι σημαντικό να κατανοήσουμε τις διαφορές μεταξύ της αίσθησης υποξίας και της αίσθησης ισχαιμίας. Παρά τη δυσκολία στην αποσαφήνιση της βιολογικής επίδρασης κάθε παράγοντα, το μοντέλο υποαιμάτωσης μας είναι φυσιολογικά εύλογο, μιμούμενο την παθολογική κατάσταση in vivo. Δεύτερον, η κατασκευή ενός μοντέλου καλυπτρίδας απαιτεί δεξιότητα και εξάσκηση, καθώς η πλειονότητα των κυττάρων αποσπώνται περιστασιακά κατά την αφαίρεση μιας καλυπτρίδας, ειδικά όταν χρησιμοποιείται η παραδοσιακή μέθοδος (Εικόνα S2a). Αυτό το ζήτημα εξαρτιόταν από την κυτταρική γραμμή που χρησιμοποιήθηκε. Για παράδειγμα, ήταν δύσκολο για εμάς να εφαρμόσουμε ένα μοντέλο καλυπτρίδας σε κελιά HEK 293 επειδή η πρόσφυσή τους σε μια καλυπτρίδα ήταν σχετικά ασθενής. Τρίτον, ήταν επιθυμητό να ελαχιστοποιηθεί η βλάβη στα καλλιεργημένα κύτταρα κάτω από μια καλυπτρίδα. Ο αριθμός των κατεστραμμένων κυττάρων αυξήθηκε όσο αυξανόταν η περίοδος κατά την οποία καλύφθηκαν, όπως φαίνεται από την ανάλυση της απόπτωσης. Προσδιορίσαμε ότι 3 ώρες ήταν κατάλληλες για την εκτίμηση του δακτυλίου HIF όταν φαινόταν να είναι στατικό και περίπου μόλις το 10 τοις εκατό των κυττάρων έγιναν αποπτωτικά (Εικόνα S11). Ο τέταρτος περιορισμός ήταν η δυσκολία σύνδεσης καλλιεργημένων κυττάρων σε μια καλυπτρίδα με ομοιόμορφο τρόπο σε κάθε δείγμα (Εικόνα S2b,c). Η διαφορά στην προσκόλληση μεταξύ μιας παραδοσιακής και μιας εναλλακτικής μεθόδου κατασκευής ενός μοντέλου καλύμματος-χειλών θα μπορούσε επίσης να επηρεάσει τη μελέτη. Μετρήσαμε το εύρος της τάσης οξυγόνου ισοδύναμο με τον δακτύλιο HIF με μια τεχνική διάρκειας ζωής φωσφορισμού, στην οποία δημιουργήσαμε ένα μοντέλο καλυπτρίδας χρησιμοποιώντας μια παραδοσιακή μέθοδο. Δεδομένου ότι ο δακτύλιος HIF κατά τη διάρκεια της ανοσοκυτταροχημείας απεικονίστηκε χρησιμοποιώντας μια εναλλακτική μέθοδο, η πραγματική τάση οξυγόνου μπορεί να είναι διαφορετική. Ελαχιστοποιήσαμε αυτά τα σφάλματα χρησιμοποιώντας την απόδειξη ότι η πιμονιδαζόλη ήταν θετική στα 10 mmHg ή λιγότερο της τάσης οξυγόνου. Ο πέμπτος περιορισμός είναι ότι το ενδοκυτταρικό pH δεν είναι απαραίτητα το ίδιο με το pH του μέσου καλλιέργειας. Αρκετές προηγούμενες αναφορές έχουν δείξει ότι το ενδοκυτταρικό pH είναι συμβατό με το pH του μέσου σε κάποιο βαθμό σε καλλιεργημένα κύτταρα (Michl et al., 2019), θα μπορούσαμε να αξιολογήσουμε μόνο την τάση στο ενδοκυτταρικό pH αλλάζοντας το pH του μέσου. In vivo, η σχέση μεταξύ του pH των ενδοκυτταρικών και εξωκυτταρικών περιοχών, όπως τα ούρα ή το σωματικό υγρό, είναι πιο περίπλοκη από ότι στα καλλιεργημένα κύτταρα. Έτσι, περαιτέρω μελέτες σχετικά με τον τρόπο με τον οποίο η μετατόπιση του pH ρυθμίζει τη συσσώρευση της πρωτεΐνης HIF-1 in vivo θα είναι απαραίτητες για το μέλλον.

Οφέλη Cistanche: βελτίωση νεφρόλειτουργία
Ένας άλλος περιορισμός είναι ότι το pH θα πρέπει να έχει επίδραση στον δείκτη υποξίας, την πιμονιδαζόλη. Συγκρίναμε την απόσταση της άκρης της θετικής στην πιμονιδαζόλη περιοχής από το κέντρο μιας καλυπτρίδας υπό διαφορετικές συνθήκες pH στο μοντέλο καλυπτρίδας μας. Το άκρο της θετικής στην πιμονιδαζόλη περιοχής ήταν συγκρίσιμο μεταξύ ρΗ 6,5, 7,4 και 8,5 (Εικόνα S12a,b). Μια προηγούμενη μελέτη έδειξε επίσης τη διατήρηση της δέσμευσης της πιμονιδαζόλης σε διαφορετικές τιμές pH (Kleiter et al., 2006). Με βάση αυτά τα στοιχεία, καταλήξαμε στο συμπέρασμα ότι η πιμονιδαζόλη είναι ο κατάλληλος δείκτης υποξίας για τα πειράματά μας καλυπτρίδας. Ο τελικός περιορισμός είναι ότι δεδομένου ενός εύρους τάσης οξυγόνου μεταξύ περίπου 4 mmHg και 20 mmHg (0,52 τοις εκατό O2 έως 2,6 τοις εκατό O2) του δακτυλίου HIF, οι Pt(II)- και Pd(II)-πορφυρίνες, οι οποίες χρησιμοποιούνται ευρέως ως βιολογικές Οι ανιχνευτές οξυγόνου έχουν πλεονεκτήματα για τη μέτρηση πολύ χαμηλών συγκεντρώσεων οξυγόνου λόγω της σημαντικά μεγαλύτερης διάρκειας ζωής φωσφορισμού τους σε σύγκριση με αυτούς που χρησιμοποιούν σύμπλοκα Ir(III) (Yoshihara et al., 2017). Ωστόσο, γενικά, μια ποσοτική μέτρηση οξυγόνου με βάση τον φωσφορισμό, που υπολογίζεται χρησιμοποιώντας την εξίσωση Stern–Volmer, έχει καλύτερη απόδοση σε χαμηλές περιοχές O2 (Papkovsky & Zhdanov, 2016). Αρκετές προηγούμενες μελέτες έχουν δείξει τη μέτρηση με βάση το σύμπλοκο Ir(III) των τάσεων οξυγόνου τόσο χαμηλές όσο περίπου 10 mmHg (Akiyama et al., 2018· Yoshihara et al., 2015). Επομένως, πιστεύουμε ότι το εύρος της τάσης οξυγόνου του δακτυλίου HIF πρέπει να είναι ένα ακριβές αποτέλεσμα.
5|ΣΥΜΠΕΡΑΣΜΑΤΑ
Συνοπτικά, διαπιστώσαμε ότι η κατανόηση των ρόλων τόσο του οξυγόνου όσο και του pH είναι απαραίτητη για την κατανόηση της φυσιολογικής κατάστασης του HIF-1 στη ΧΝΝ και μπορεί να επιτευχθεί με τη διερεύνηση των σωληναριακών κυττάρων με υποαιμάτωση. Το μοντέλο καλυπτρίδας, με τους περιορισμούς του στην εισροή μέσων, ήταν ένα καλό μοντέλο υποαιμάτωσης in vivo, ειδικά στα σωληνάρια στη ΧΝΝ, καθώς η αραίωση των περισωληνωδών τριχοειδών αγγείων είναι κύριο χαρακτηριστικό της ΧΝΝ (Mimura & Nangaku, 2010; Nangaku, 2006). Αυτό το μοντέλο υποαιμάτωσης μπορεί επίσης να μιμηθεί τις διαβαθμίσεις οξυγόνου και pH in vivo, όπως όγκους και ισχαιμικές βλάβες. Το μοντέλο παρέχει μια πολλά υποσχόμενη προσέγγιση για την αποσαφήνιση αυτών των βιολογικών μηχανισμών.
ΣΥΓΚΡΟΥΣΗ ΣΥΜΦΕΡΟΝΤΩΝ
Όλοι οι συγγραφείς δεν έχουν να δηλώσουν σύγκρουση συμφερόντων.
ΣΥΝΘΗΚΕΣ ΣΥΓΓΡΑΦΕΩΝ
Όλοι οι συγγραφείς συνέβαλαν στη διαμόρφωση της συνολικής ιδέας. Ο TH πραγματοποίησε τα συνολικά πειράματα. Οι TH και YH ανέλυσαν τα αποτελέσματα και έκαναν τα νούμερα. Θ. έγραψε το πρωτότυπο χειρόγραφο. Οι KM, TY και ST πραγματοποίησαν το πείραμα χρησιμοποιώντας μια τεχνική φωσφορισμού διάρκειας ζωής και επεξεργάστηκαν το μέρος του χειρογράφου. Οι YH, TT και MN επεξεργάστηκαν το συνολικό χειρόγραφο. Όλοι οι συγγραφείς έχουν διαβάσει και εγκρίνει το τελικό χειρόγραφο.
ΑΝΑΦΟΡΑ
Akiyama, H., Takahashi, I., Shimoda, Y., Mukai, R., Yoshihara, T., & Tobita, S. (2018). Απεικόνιση οξυγόνου βασισμένη σε σύμπλοκο Ir(iii) ζωντανών κυττάρων και οφθαλμικού βυθού με κλειστή κάμερα ICCD. Photochemical and Photobiological Sciences, 17(6), 846–853.
Akizawa, T., Nangaku, M., Yamaguchi, T., Arai, M., Koretomo, R., Maeda, K., Miyazawa, Y., & Hirakata, H. (2019). Enarodustat, θεραπεία μετατροπής και συντήρησης για την αναιμία σε ασθενείς που υποβάλλονται σε αιμοκάθαρση: Μια τυχαιοποιημένη, ελεγχόμενη με εικονικό φάρμακο δοκιμή φάσης 2b ακολουθούμενη από μακροχρόνια δοκιμή. Nephron, 143(2), 77–85.
Ameri, K., Burke, B., Lewis, CE, & Harris, AL (2002). Ρύθμιση ενός στοιχείου VL30 αρουραίου σε ανθρώπινα καρκινικά κύτταρα μαστού σε υποξία και ανοξία: Ρόλος του HIF-1. British Journal of Cancer, 87(10), 1173-1181.
Asai, H., Hirata, J., Hirano, A., Hirai, K., Seki, S., & Watanabe- Akanuma, M. (2016). Η ενεργοποίηση του υποδοχέα υδρογονάνθρακα αρυλίου μεσολαβεί στην καταστολή της επαγόμενης από υποξία εξαρτώμενης από παράγοντα έκφρασης ερυθροποιητίνης από θειικό ινδοξύλιο. American Journal of Physiology. Cell Physiology, 310(2), C142-C150.
Burke, TJ, Malhotra, D., & Shapiro, JI (1999). Παράγοντες που διατηρούν μια κλίση pH εντός του νεφρού: ρόλος της αρχιτεκτονικής των αγγείων. Kidney International, 56(5), 1826–1837.
Carrera, S., Senra, J., Acosta, MI, Althubiti, M., Hammond, EM, de Verdier, PJ, & Macip, S. (2014). Ο ρόλος του μεταγραφικού παράγοντα HIF-1άλφα στην αυξημένη κυτταρική διαίρεση σε φυσιολογικές τάσεις οξυγόνου. PLoS One, 9(5), e97938.
Chen, N., Hao, C., Peng, X., Lin, H., Yin, A., Hao, L., Tao, Y., Liang, X., Liu, Z., Xing, C., Chen, J., Luo, L., Zuo, L., Liao, Y., Liu, BC, Leong, R., Wang, C., Liu, C., Neff, T., … Yu, KHP (2019 ).
Roxadustat για αναιμία σε ασθενείς με νεφρική νόσο που δεν υποβάλλονται σε αιμοκάθαρση. New England Journal of Medicine, 381(11), 1001-1010.
Chen, N., Qian, J., Chen, J., Yu, X., Mei, C., Hao, C., Jiang, G., Lin, H., Zhang, X., Zuo, L., He, Q., Fu, P., Li, X., Ni, D., Hemmerich,S., Liu, C., Szczech, L., Besarab, A., Neff, TB, … Valone, F.
Η. (2017). Μελέτες Φάσης 2 του στοματικού επαγόμενου από την υποξία αναστολέα του παράγοντα προλυλ υδροξυλάσης FG-4592 για τη θεραπεία της αναιμίας στην Κίνα. Nephrology, Dialysis, Transplantation, 32(8), 1373–1386.
Chiang, CK, Tanaka, T., Inagi, R., Fujita, T., & Nangaku, M. (2011). Το θειικό ινδοξύλιο, μια αντιπροσωπευτική ουραιμική τοξίνη, καταστέλλει την παραγωγή ερυθροποιητίνης με τρόπο που εξαρτάται από το HIF. Laboratory Investigation, 91(11), 1564–1571.
Chun, WJ, Nah, DY, Bae, JH, Chung, JW, Lee, H., & Moon, IS (2015). Το διάλυμα γλυκόζης-ινσουλίνης-καλίου προστατεύει τα κοιλιακά μυοκύτταρα νεογνών αρουραίων σε ένα μοντέλο in vitro ισχαιμίας/επαναιμάτωσης καλυπτρίδας. Korean Circulation Journal, 45(3), 234–241.
Coyne, DW, Goldsmith, D., & Macdougall, IC (2017). Νέες επιλογές για την αναιμία της χρόνιας νεφρικής νόσου. Kidney International Supplement, 7(3), 157–163. φιλί.2017.09.002
Deng, Α., Arndt, ΜΑ, Satriano, J., Singh, Ρ., Rieg, Τ., Thomson, S. et al (2010). Προστασία των νεφρών σε χρόνια νεφρική νόσο: ενεργοποίηση παραγόντων που προκαλείται από υποξία έναντι αποκλεισμού της αγγειοτενσίνης II. American Journal of Physiology. Renal Physiology, 299(6), F1365–F1373.
Filatova, A., Seidel, S., Bogurcu, N., Graf, S., Garvalov, BK, & Acker, T. (2016). Η οξέωση δρα μέσω του HSP90 με τρόπο ανεξάρτητο από το Ph.D./VHL για να προάγει τη λειτουργία του HIF και τη διατήρηση των βλαστοκυττάρων στο γλοίωμα. Cancer Research, 76(19), 5845-5856. ΜΠΟΡΩ-15-2630
Goldfarb, M., Rosenberger, C., Abassi, Z., Shina, A., Zilbersat, F., Eckardt, KU, Rosen, S., & Heyman, SN (2006). Οξεία επί χρόνια νεφρική ανεπάρκεια στον αρουραίο: λειτουργική αντιστάθμιση και ανοχή στην υποξία. American Journal of Nephrology, 26(1), 22–33.
Heyman, SN, Rosenberger, C., Rosen, S., & Khamaisi, M. (2013). Γιατί ο σακχαρώδης διαβήτης αποτελεί παράγοντα κινδύνου για νεφροπάθεια που προκαλείται από σκιαγραφικό; BioMed Research International, 2013, 123589.
Hirakawa, Y., Mizukami, K., Yoshihara, T., Takahashi, I., Khulan, P., Honda, T., Mimura, I., Tanaka, T., Tobita, S., & Nangaku, M. (2018). Η ενδοβιολογική απεικόνιση φωσφορισμού εφ' όρου ζωής του νεφρικού φλοιού μετρά με ακρίβεια τη νεφρική υποξία. Kidney International, 93(6), 1483–1489.
Hirakawa, Y., Tanaka, T., & Nangaku, M. (2017). Νεφρική υποξία σε ΧΝΝ. Παθοφυσιολογία και μέθοδοι ανίχνευσης. Σύνορα στη Φυσιολογία, 8, 99.
